В настоящее время в промышленном масштабе производяться азотные (аммиачная селитра, карбамид, сульфат аммония, натриевая и кальциевая селитры), фосфорные (простой и двойной суперфосфаты), калийные (хлорид и сульфат калия), а также комплексные и сложно-смешанные удобрения (нитроаммофос, нитроаммофоска, фосфаты аммония) минеральные удобрения.
Комплексные (многосторонние) удобрения содержат два или три основных питательных компонента (азот, фосфор, калии), а иногда и другие (магнии, кальции, серу, микроэлементы).
Их выпускают в форме твердых (сложные, сложно-смешанные) или жидких (ЖКУ) продуктов. Технологии их производства и основные процессы в общих чертах сходны.
Гранулийрованные комплексные удобрения получают либо кислотной переработкой природных фосфатов с получением азотосодержащей пульпы, либо аммонизацией кислот, полученных на отдельных линиях (аммофос, нитроаммофос).
Нейтрализованные пульпы при необходимости смешивают с калийным компонентом. Извлечение фосфора из руды проводят аналогично процессу получения фосфорной кислоты или пульпы двойного суперфосфата. Дальнейшую переработку осуществляют по нескольким технологическим схемам, принципиально отличающимся способом предварительного удаления влаги.
Из комплексных удобрении наиболее распростронены сложные. К ним относятся одинарные соли, содержащие несколько питательных элементов или композиции из солей, включающих два (N+K, N+P, P+K) или три (N+K+P) питательных элемента.
В сельском хозяйстве используется свыше 10 марок усавершенствоанных комплексных удобрении. Все комплексные удобрения являются высококонцентрированными и применение их более эффективно, чем применение простых удобрении. Этим обусловлено интенсивное расширение производства и потребления сложных комплексных удобрении.
Раздел 1. Физико — химическая характеристика процесса.
1.1 Методы производства получения жидких комплексных и сложно-смешанных удобрении
К комплексным удобрениям относятся сложные, сложно-смешанные удобрения, выпускаемые в виде гранул, а также жидкие комплексные. Ниже излагаются основные способы производства сложных удобрении, получивших широкое распростронение в нашей стране.
Все сложные минеральные удобрения по методу их производства могут быть разделены на три группы:
- удобрения, получаемые переработкой фосфорной кислоты (аммофос, диаммофос);
- удобрения, получаемые переработкой смеси фосфорной и азотной кислоты (нитроаммофос, нитроаммофоска);
- удобрения, получаемые разложением природных фосфатов азотной кислотой (нитрофос, нитроаммофоска);
- Таким образом, некоторые удобрения, например, нитроаммофоска, могут быть получены различными методами.
Жидкие комплексные удобрения (ЖКУ) получают методами горячего и холодного смешения.
Производство нитроаммофоски
... отвечать требованиям и нормам, указанным в табл. I-1. [3] Производство нитроаммофоски При получении комплексных удобрений - нитрофосов и нитрофосок- азотным разложением фосфатов азотная кислота является источником не только ... непрерывно поступает на гранулирование и сушку в аппарат 14 (БГС или сферодайзер, работа сферодайзера основана на том же принципе, что и БГС, но без внутреннего ...
горячего смешения
Наибольшее развитие получило производство ЖКУ состава 10-34-0 (ТУ 6-08-414-78) на основе экстракиционной полифосфосфорной кислоты со степенью конверсии Р 2 О5 не менее 55%. На основе полифосфорной кислоты можно получить растворы ЖКУ с низкой температурой кристаллизации 18-200 С и малой вязкостью (не более 50 Мпа·с при 200 С).
холодного смешения
Производство аммофоса можно строить по различным технологическим схемам, различающимся концентрацией используемой фосфорной кислоты и конструкцией аппаратуры:
На основе разбавленной экстракиционной кислоты:
- с сушкой пульпы в распылительной сушилке;
- с упариванием пульпы в вакуум-выпарных аппаратах и сушкой в аппарате БГС;
- с сушкой пульпы и грануляцией ее в распылительной сушилке-грануляторе кипящего слоя РКГС;
На основе концентрированной фосфорной кислоты:
- с грануляцией и сушкой продукта в аммонизаторе-грануляторе АГ;
- с самоиспарением пульпы под давлением и сушкой в барабанном грануляторе-сушилке-холодильнике БГСХ;
— Технологическая схема производства аммофоса с использованием аппарата РКСГ позволяет соединить в одном аппарате операции упаривания пульпы, грануляции и сушки продукта, что обеспечивает высокую интенсивность всех стадии процесса при малых затратах тепла и электроэнергии.
тукосмешением
Обычно смешенные удобрения получают на небольших тукосмесительных установках (ТСУ) местного значения. Процесс их приготовления состоит их следующих последовательно осуществляемых операции: 1)подготовка удобрении к смешению в ТСУ; 2) дозирование; 3) смешение; 4) выгрузка тукосмесей.
Сложно-смешанные удобрения получают в результате смешения готовых односторонних удобрении и полупродуктов, а также серной и фосфорной кислот с одновременной аммонизацией смеси газообразным аммиаком или аммиакатами. При этом протекают химические реакции, которые способствуют улучшению качества удобрения, получению более однородных и прочных гранул продукта.
Сложно-смешанные, как и сложные удобрения, можно длительное время хранить до внесения в почву, что дает возможность производить их в промышленных мастабах. Согласно ГОСТу в нашей стране предусмотрен выпусксложно-смешанных гранулийрованных удобрении на основе простого супефосфата, аммиачной селитры и хлорида калия или простого суперфосфата и хлорида калия со следующими соотношениями:
|
Соотношение N : Р 2 О5 : K2 O |
Состав, % | |||
| N | Р 2 О5 | K 2 O | N + Р 2 О5 +K2 O | |
|
1:1:1 0:1:1 1:1,5:1 1:1:1,5 1:1:5-0 |
10-11 — 7-8 9-10 10-11 |
10-11 13-14 11-12 9-10 15-16 |
10-11 13-14 7-8 14-15 — |
30-33 26-28 25-28 32-35 25-27 |
Идеальным компонентом для сухого тукосмешения является гранулийрованный аммофос. В настоящее время и в перспективе аммофос остается основой для производства смешанных комплексных удобрении. Для розничной торговли выпускаютс удобрительные тукосмеси с добавкой бора или магния.
1.2 Теоретические основы принятого метода
1.2.1 Производство аммофоса
Ведущее место среди комплексных удобрении занимает аммофос, являющийся универсальным удобрением, которое используют как для внесения в почву, так и для изготовления минеральных удобрении смешанного типа.
Аммофос принадлежит к числу сложных удобрении, получаемых в наибольшем количестве.
В основе производства аммофоса лежит гетерогенные экзотермический процесс нейтрализации фосфорной кислоты газообразным аммиаком:
Н 2 РО3ж + NН3г = NН4 Н2 РО4т ∆ Н ,
∆ Н = 147 кДж
Процесс ведут при избытке аммиака, поэтому в системе, наряду с реакцией образования моноаммонийфосфата, частично протекает реакция образования диаммонийфосфата:
Н 2 РО3 + 2NН3 = (NН4 )НРО4 — ∆ Н ,
∆ Н = 75,4 кДж
в результате чего в составе готового продукта содержится до 10% диаммонийфос-фата.
Аммофос представляет двойное (N+P) сложное комплексное удобрение, содержащее в качестве основного вещества моноаммонийфосфат NН 4 Н2 РО4 и примесь (до 10%) диаммонийфосфата (NН2 )2 РО4, образующегося в процессе получения. Моно- и диаммонийфосфаты представляют собой твердые кристаллические вещества, малогигроскопичные, растворимые в воде. Из фосфа-тов аммония моноаммонийфосфат термически наиболее устойчив и при нагревании до 100-1100 С практически не разлагается. Диаммонийфосфат, и особенно триаммонийфосфат при нагревании доссоциируют с выделением аммиака, например:
(NН 2 )2 РО4 = NН4 Н2 РО4 + NН3
Режим процесса нейтрализации выбирают так, чтобы обеспечить получение достаточно подвижной и способной к перекачиванию по трубопроводам аммофосной пульпы. Вязкость пульпы зависит от концентрации исходной кислоты, растворимости фосфатов аммония и температуры.
1.2.2. Производство сложно-смешанных удобрении
Производство смешанных удобрении преследует задачу получения уравновешенных двойных или тройных удобрении из простых или неуравновешенных сложных удобрении. Сложно-смешанные удобрения готовят с добавлением некоторых реагентов и полупродуктов (фосфорной и серной кислота, аммиак и аммиакаты, концентрированные растворы удобрении -так называемые «плавы»).
Основные химические реакции при производстве сложно-смешанных удобрении протекают аммонизаторе-грануляторе, где исходные компоненты взаимодействуют с аммиаком:
H 3 PO4 + NH3 = NH4 H2 PO4
Ca(H 2 PO4 )2
- H2 O + NH3 = CaHPO4 + NH4 H2 PO4 + H2 O
NH 4 H2 PO4 + CaSO4 + NH3 = CaHPO4 + (NH4 )2 SO4
KCl + NH 4 NO3 = KNO3 + NH4 Cl
Водорастворимый Са(H 2 PO4 )2, содержащийся в суперфосфате, частично превращется в менее растворимый CaHPO4. Ретроградацию предотвращают путем введения в смесь серной или фосфорной кислоты:
Ca(H 2 PO4 )2 + H2 SO4 + 2NH3 = CaSO4 + 2NH4 H2 PO4
При получении смешанных удобрении следует учитывать, что между некоторыми удобрениями могут идти нежелательные химические процессы, в результате которых будут утрачены питательные вещества и ухудшены физические свойства удобрения. Например, при смешении аммиачной селитры с суперфосфатом в результате протекания реакции:
NH 4 NO3 + H3 PO4 = NH4 H2 PO4 + HNO3
2NH 4 NO3 + Ca(H2 PO4 )2 + Ca(NO3 )2
часть азота теряется в виде паров азотной кислоты или оксидов азота, а физические свойства смеси ухудшаются из-за образования гигросопичного нитрата кальция. Введение в эту смесь нейтрализирующих добавок предотвращает выделение азотной кислоты, способствует превыщению части монокальцийфосфата и дикальцийфосфат, что улучшает физические свойства удобрения.
Получение качественных тукосмесей достигается правильным подбором компонентов и использованием для смешения удобрении с определенными свойствами. При непрвильном подборе компонентов возможно ухудшение физических свойствтукосмеси или потери питательных веществ. Поэтому при смешении, во избежание нежелательных явлений, обычно рекомендуется пользоваться специальными диаграммами и таблицами смесимости.
Наприамер на диаграмме 1 , показано, что калийные соли можно смешивать со всеми удобрениями, аммофос -со всеми удобрениями, кроме металлургических шлаков, аммиачную селитру нельзя смешивать с карбамидом и тд.
Однако эти таблицы и диаграммы не учитывают влияние нейтрализирующих добавок, изменений в ассортименте и качестве удобрении; рекомендации таблиц относятся только к парным комбинациям и, следовательно, не могут быть использованы при получении трехкомпонентных систем.
Возможный состав смешанных удобрении
| Компоненты | Состав удобрений, масс. % | Соотношения N : Р 2 О5 : K2 O | |||
| N | Р 2 О5 | K 2 O | N + Р 2 О5 +K2 O | ||
|
Аммиачная селитра, аммофос, суперфосфат двойной, хлорид калия Карбамид, аммофос, хлорид калия Аммофос, аммиачная селитра, хлорид калия Суперфосфат двойной, аммиач-ная селитра, хлорид калия, нейтрализирующий добавки |
16 19,3 15,4 17,2 13,9 |
16 19,3 30,8 17,2 13,9 |
16 19,3 15,4 17,2 13,9 |
48 57,9 61,6 51,6 41,7 |
1:1:1 1:1:1 1:2:1 1:1:1 1:1:1 |
1.3 Физико-химические свойства сырья, вспомогательных материалов и готовой продукции
Жидкие комплексные
Жидкие комплексные удобрения по сравнению с твердыми комплексными удобрениями имеют ряд преимуществ, поютому объем их производства за последние годы значительно возрос. Использование ЖКУ позволяет полностью механизировать процесс внесения удобрения в почву, обеспечивает равномерное распределение действующих веществ, создает возможность одновременного внесения с удобрениями гербицидов, пестицидов, микроэлементов. При производстве ЖКУ значительно снижаются капитальные затраты и стоимость переработки сырья, так как в технологической схеме отсутствуют стадии сушки, гранулирования, охлаждения, дробления, рассева, кондиционирования и большое число транспортных средств.
Качество и стабильность растворов ЖКУ зависят от степени конверсии Р 2 О5
и содержания примесей железа и алюминия в полифосфорной кислоте. При увеличении степени конверсии и уменьшении содержания примесей в кислоте, качество и стабильность растворов повышаются. Из кислоты, содержащей до 1% Аl 2 O3 или 1,5% Fe2 O3, получаются прозрачные и стабильные ЖКУ марки 10-34-0. При приготовлении аналогичных ЖКУ из более загрязненной килоты, из растворов выпадает нерастворимый осадок черного цвета, представляющий собой аммонийные пирофосфаты железа и аллюминия.
Состав и свойства ЖКУ
|
Показатели |
Жидкие комплексные удобрения | |||
| 01:01:01 | 1,5:1:1 | 1:1,5:1 | 01:01:01,50 | |
|
Содержание питательных веществ (сумма), масс.% Содержание, % Р 2 О5 общ. Р 2 О5 орто. N общ. К 2 О Степень конверсии, % рН Плотность при 20 0 С, кг/м3 Вязкость при 20 0 С, Мпа·с Температура замерзания, 0 С |
28,15 9,15 5,11 9,59 9,41 44,2 6,8 1264 25,4 -18 |
27,61 7,53 4,42 11,87 8,21 41,3 6,77 1250 23 -2,3 |
31,23 13,01 6,96 9,48 8,72 46,5 7,13 1290 39,4 -20 |
25,86 7,61 4,06 7,41 10,84 46,7 6,63 1240 18,2 -14 |
Аммофос. Стандартный аммофос в зависимости от состава исходной экстракиционной фосфорной кислоты содержит от 35,5 до 50% усвояемой Р2 О5 водорастворимой и от 9 до 11% азота. Выпускается в порошковидном и гранулированном состоянии.
Экстракционная фосфорная кислота.
Аммиак.
Исходные компоненты сложно-смешанных удобрении.
Исходные компоненты должны содержать минимальное количество влаги, не слеживаться, иметь одинаковый гранулометрический состав и быть негигроскопичными. Кроме того, используемые в сухом тукосмешении простые и неуравновешенные комплексные удобрения должны сохранять сыпучесть, неслеживаемость и гранулометрический состав в процессе их транспортирования в специальных вагонах с донной выгрузкой и при хранении насыпью в течении 6 месяцев.
Характеристика гранулометричсекого состава исходных компонентов
удобрении для тукосмесей
|
Исходное удобрение |
Размер гранул, мм |
Плот-ность, т/м 3 |
Форма гранул | ||||
| 3,3 | 2,4-3,3 | 1,65-2,4 |
1- 1,65 |
до 1 | |||
| Содержание фракции, % | |||||||
|
Аммиачная селитра Карбамид гранулированный Сульфат аммония Аммонитрофос (30-10-0) Диаммонийфосфат (18- 46-0) Двойной суперфосфат Хлорид калия гранулированный в рас- воре прессованный в дроб- леный |
0 0 1 0 0 0 0 0 1 0 0 |
6 0 35 25 1 6 5 5 29 5 14 |
65 8 54 43 17 46 63 83 56 29 65 |
25 89 8 28 78 41 31 12 13 58 20 |
4 3 2 4 4 7 1 0 1 8 1 |
1,29 1,65 1,50 1,63 1,32 1,64 1,27 1,63 2,12 1,93 1,96 |
Правильная шарообразная Очень правильная шаро- образная Относительно шарообразная Неправильные чешуйки Очень правильная шаро- образная Неправильные чешуйки Правильная шарообразная То же Относительно шарообразная То же Неправильная |
От качества исходных компонентов тукосмесей напрямую зависит качество сложно-смешанных удобрении. Чем выше качество исходных компонентов, тем лучше свойства удобрении (срок годности, неслеживаемость и тд.).
Тукосмеси.
Одним из главных требований к качеству сложно-смешанных удобрении является однородность химического состава. Однородность сложно-смешанных удобрении достигается использованием для смешения удобрении, близких по гранулирометрическому составу, и тщательность их перемешивания. Требования к физико-химическим и механическим свойствам тукосмесей определяются многими факторами — планируемыми объемами тукосмешения, сроками и методами их приготовлении, уровнем механизации процесса тукосмешения, схемой транспортирования тукосмесей до поля и дт. Одним их главных требовании предъявляемых к тукосмесям на основе гранулированных компонентов, является получение хорошо сыпучих, неслеживающихся пригодных к механическому рассеву продуктов.
Требования к химическому составу и концентрации питательных веществ в тукосмесях удовлетворяется соответствующим подбором исходных компонентов. Сохранение сыпучести и прочности гранул тукосмеси обеспечивается минимально допустимым содержанием влаги в исходных компонентах.
Физико-химические свойства компонентов тукосмесей
|
Удобрение |
Влаж- ность, % |
Гигро-скопичес-кая точка при 25 0 С, % |
Слежива-емость, кПа |
Содер-жание гранул 1-4 мм, % |
Статистическая прочность гранул, МПа |
Сыпучесть Н/с |
|
Аммиачная селитра Карбамид Простой суперфосфат Двойной суперфосфат Хлорид калия (пресс.) Хлористый калии (круп- нозерн.) Аммофос Нитрофос Нитроаммофос Карбоаммосфос(опытная партия) Полифосфат аммония (опыт. партия) |
0,1-0,3 0,1-0,3 2,7-3,6 2,7-3,8 0,2-0,6 0,2-0,5 0,4-0,8 0,6-1,0 0,7-1,0 0,2-0,6 0,4-1,3 |
59 — 64 72 — 74 64 — 68 60 — 64 62 — 69 68 — 74 68 — 74 58 — 61 56 — 58 51 — 60 58 — 65 |
1-10 2 0 0 10-20 40 0 100 60-70 0,1-0,2 0,02 |
95 — 98 95 — 98 90 — 93 80 — 90 80 — 85 43 — 66 95 — 99 95 — 96 95 — 97 90 — 99 74 — 98 |
0,8 — 3,0 0,8 — 1,6 0,1 — 2,3 1,5 — 3,4 3,0 — 5,8 — 3,0 — 11,0 3,0 — 10,0 2,1 — 4,6 20 — 90 40 — 105 |
0,70-0,86 0,70-0,72 0,60-0,68 0,60-0,62 0,80-0,83 1,00-1,20 0,70-0,78 0,56-0,60 0,75-0,85 58-68 6472 |
| П р и м е ч а н и е: влажность удобрении определяли по ГОСТ 20851.4-75, слеживаемость — по ГОСТ 21560.2-76, гранулометрический состав — 21560.1-75, статистическая прочность — ГОСТ 21560.2-76, гигроскопические точки — экстракиционным методом, сыпучесть — по скорости истечения удобрения из воронки отверстия диаметром 20 мм. | ||||||
Наиболее сильное влияние на на слеживаемость удобрении оказывает содержание в них влаги. В найбольшей степени слеживаемости подвергаются водорастворимые соли. Следствием повышенной влажности является снижение механической прочности гранул, деформация и увеличение площади контакта между ними.
Для всех марок удобрении содержание воды должно быть не более 1%, статистическая прочность гранул не менее 2 МПа. Замена простого суперфофата на двойной повышает сумму питательных веществ в готовом удобрении с 30-33 до 42-44%. В случае применения фосфорной кислоты концентрация питательных веществ увеличивается соответственно до 38 и 48%. Еще более концентрированные сложно-смешанные удобрения (до 58% питательных веществ) получают на основе аммофоса или диаммифоса, аммиачной селитры и хлорида калия.
Изменение температурного режима хранения приводит к ускорению процессов рекристализации с образованием внешнего кристалического каркаса и солевых мостиков между частицами, химический состав которых зависит от состава солей, входящих в данное удобрение.
В процессе приготовления, хранения, транспортирования и внесения тукосмесейнеобходимо свести к минимуму потери питательных веществ и их превращение в менее усвояемые формы. Наибольшая сохранность грануло-метрического состава удобрении при их транспортировании и погрузочно-разгрузочных работах обеспевиается при статистической простности гранул не менее 2,0 МПа.
Некоторые марки сложно-смешанных удобрении, способные сравнительно длительное время храниться без расслаивания, могут выпускаться предприятиями химической промышленностью. Например, путем прессования ретура простого суперфосфата и кристаллического хлорида калия получают РК -тукосмесь состава 0-14-14. согласно ГОСТу в смеси допускается содержание не более 2% влаги и свободной Р 2 О5 не менее 90% гранул размером 1- 4 мм и не более 5% частиц менее 1 мм. Механическая прочность гранул не ниже 3,5 — 4 МПа. Гарантийный срок хранения такой смеси 6 месяцев. Продукт имеет хорошие физические свойства, что позволяет его хранить и транспортировать не только в мешках, но и насыпью.
Гранулированные сложно-смешанных удобрения способны к расслаиванию (сегрегации) при транспортировании и хранении насыпью, поэтому их предпочитают доставлять на поля специальным автотранстпортом.
Вспомогательные материалы., Аммиачная вода -, Вода для охлаждения —
Пар —
Горячие топочные газы —
Раздел 2. Технологические и эксплуатационные характеристики процесса
2.1 Технологическая схема производства ЖКУ состава 10-34-0 из экстракиционной полифосфорной кислоты.
Предварительно подогретая полифосфорная кислота поступает в приемныйй сборник кислот 10, откуда через промежуточную емкость 15 при 70 0 С непрерывно подается в трубчатый реактор 3 для нейтрализации газообразным аммиаком. Мольное отношение исходных компонентов NH3 : Р2 О5 = 2 : 2,2. Аммиак поступает по центральному вводу реактора в количестве 60% от общего расходаю за счет тепла нейтрализации температура в реакторе повышается до 280-3200 С, благодаря чему происходит дальнейшая дегидратация полифорной кислоты и степень конверсии Р2 О5 увеличивается.
Образующийся плав полифосфатов аммония поступает в донейтрализатор 4, где растворятся в аммийачной воде и нейтралийзуется аммиаком до рН=6-7. Температуру в донейтрализаторе поддерживают в пределах 60-70 0 С, за счет подачи охлаждающей воды в рубашку аппарата и непрерывной циркуляции раствора через холодильник 5. Из донейтрализатора выводят готовый раствор ЖКУ состава10-34-0. Его охлаждают в водном холодильнике до 25-300 С и направляют на склад. Пары воды и непрореагировавший аммиак из донейтрализатора направляют в адсорбер 13 с плавающей кольцевой насадкой, орошаемой водой. Очищенные газы выбрасывают в атмосферу, а образующийся в абсорбере аммийачную воду подают в необходимом количестве в донейтрализатор на растворение плава. Для увеличения срока службы и надежности в эксплуатации реакторы, нейтрализаторы и теплообменники изготавливают из корозийонностойких марок стали, трубчатые реакторы изготавливают из сплавов марок 06ХН28 МДТ, «халстеллой» или углеграфита. Обоудование для хранения и транспортирования из углеродистой стали.
2.2Технологическая схема производства аммофоса.
Экстракционная фосфорная кислота концентрацией 25-28% Р 2 О5 и газообразный аммиак поступают в аппарат САИ (скоростной аммнизатор-испаритель) 1 при мольном отношении NН3 :Н2 РО3 =1:1. За счет теплоты нейтрализации темепература пульпы поднимается до 1000 С и часть воды испаряется.
Затем аммофосная пульпа через промежуточные сборник 2, обогреваемй паром, подается в верхнюю часть аппарата РКСГ 3, где распыляется топочными газами, нагретыми до 700 0 С, поступающими из топки 4.
Пульпа упаривается и ее частицы опускаются в нижнюю часть аппарата, в которой топочными газами, поступающими из топки 5, создается кипящий слой. Здесь порошкообразный продукт гранулируется и высушивается. Высушенные гранулы поступают в холодильник кипящего слоя 6, в который подается воздух из холодильной установки 7, охлаждаемой жидким аммиаком.
Охлажденные гранулы аммофоса сортируются на грохоте 8. товарная продукция нужной дисперности поступает на склад, а крупная фракция измельчается в дробилке 9 и возвращается в холодильник 6. Фазы из аппарата РКСГ проходят через циклон 10, где отделяется пыль аммофоса, возвращаемая в аппарат, и поступает на абсорбцию аммиака и фтористого водорода в абсорбер 11, орошаемый водой.
2.3 Технологическая схема получения сложно-смешанных удобрении.
Производство сложно-смешанных удобрен ии можно получать различными схемами. В данной схеме представлена схема, где операции аммонизации и гранулирования осуществляются в одном аппарате -аммонизаторе-регулятое.
Исходные сухие калийные и фосфорные удобрения предварительно измельчают и смешивают в барабанном смесителе 3. Сюда же поступает ретур из бункера 1. Продолжительность смешения 2 минуты. Сухая смесь из смесителя 3 и жидкие продукты из емкостей 4 -плав аммиачной селитры или аммиакат, фосфорная и серная кислота — поступают в аммонизатор-гранулятор 9. Газообразный аммиак подают из испарителя 10 под слой гранулируемого материала.
В аммонизаторе-грануляторе протекают следующие химические реакции:
H 3 PO4 + NH3 = NH4 H2 PO4
Ca(H 2 PO4 )2
- H2 O + NH3 = CaHPO4 + NH4 H2 PO4 + H2 O
NH 4 H2 PO4 + CaSO4 + NH3 = CaHPO4 + (NH4 )2 SO4
KCl + NH 4 NO3 = KNO3 + NH4 Cl
Аммонизация и гранулироание осуществляется в течении 8-10 минут. При аммонизации суперфрсфата поддерживают отношение NH 3 : H3 PO4 = 1:3. За счет тепла реакции температура смеси в аппарате повышается до 65-750 С, при этом испаряется 30-35% введенной воды. Полученные сырые гранулы поступают в сушильный барабан 12, где они высушивются горячими топочными газами при 3000 С. Температура гранул на выходе из сушилки 70-800 С, влажность 0,5%.
Сухой продукт классифицируют га грохоте 6. Крупные частицы измельчают в дробилке 8 и возвращают на россев. Мелкую фракцию возвращают в качестве ретура в аммонизатор-регулятор. Товарную фракцию (1-3 мм) охлаждают до 30-40 0 С в аппарате 7 кипящего слоя, кондиционируют в барабане 13 и упаковывают. Отходящие газы очищают от пыли в циклонах, а от аммиака и фтора — полых башнях, орошаемых водой.
На 1 т сложно — смешанного удобрения состава 10,5 — 10,5 — 10,5 расходуется 0,54 т простого суперфосфата (19% Р 2 О5 ), 0,027 т серной кислоты 0,282 т 90%-ного плава аммиачной селитры, 0,023 т аммиака, 0,176 т хлорида калия (60% К2 О).
2.1 Средства контроля и управление технологическим процессом производства аммофоса
Основными стадиями технологического процесса получения аммофоса из неупаренной кислоты являются: ступенчатая нейтрализация кислоты аммиаком последовательно до рН 3 и 5, выделение воды из аммофосной пульпы, гранулирование продукта, сушка гранул и их сортировка по размерам частиц.
Одним из способов получения аммофоса этой группы является применение продукта последовательно в горизонтальном смесителе и окаточном барабане с окончательным высушиванием продукта в барабанной сушилке. Эта схема призвана недостаточно удовлетворительной вследствие экстенсивности работы распылительной сушилки. Более совершенен способ с применением распылительно-кипящий сушилки-гранулятора (РКСГ).
В этом аппарате совмещены процессы обезвоживания аммофосной пульпы и гранулирования аммофоса.
Для переработки неупаренной экстракиционной фосфорной кислоты разработан новый вариант производства аммофоса, включающие следующие операции: нейтрализация кислоты аммиаком в скоростном аммонизаторе-испарителе (САИ); выпаривание аммофосой пульпы в многокорпусной противоточной установке поверхностного типа с принудительной циркуляцией или в аппарате барботажно-скрубберного типа, сушка и гранулирование в барабанном грануляторе-сушилке (БГС), сортировка гранул, охлаждение товарного продукта воздухом в аппарате кипящего слоя (КС).
Концентрирование фосфорной кислоты выпариванием в методах других групп производств аммофоса предназначено не только для выделения воды, но и для обесфторивания кислоты. В процессе выпаривания может быть выделено до 80% газообразных соединении фтора. В одном из способов этой группы концентрирования фосфорнай кислота нейтрализируется газообразным аммиаком в две стадии: сначала в двух-трех сатураторах до рН 2,5-3,5, затем в барабанном аммонизаторе-грануляторе (АГ); в этом аппарате одновременно протекает процесс гранулирования с введением порошковидного ретурного аммофоса. За счет тепла нейтрализации здесь происходит частичная подсушка гранул аммофоса. Продукт окончательно высушивается в барабанной сушилке после чего гранулы сортируются и охлаждающей в аппарате КС.
Разработана также схема производства аммофосса, в которой вода, вводимая с экстракиционной фосфорной кислотой, удаляется выпариванием, а также за счет тепла реакции нейтрализации кислота аммиаком. Аммонизация кислоты происходит в трубчатом (струйном) реакторе под давлением, в котором протекает непрерывн ый процесс взаймодействия фосфортной кислоты с газообразным аммиаком. Реакция протекает с выделением тепла, поэтому температура аммофосной пульпы достигает 100-200 0 С. Пульпа из реактора вводится с помощью форсунки в закрытую башню, где давление снижается до атмосферного, в результате чего происходит самоиспарение воды за счет генерированного в пульпе тепла при этом подсушенный аммофос в виде мелкого порошка падает на дно башни. Пары воды вместе с газами и аммофосной пылью улавливаются водой в скруббере. Порошковидный аммофос гранулируется или используется для смешения с другими удобрениями.
На рисунке 1 представлена схема контроля производства аммофоса из упаренной фосфорной кислоты с применением аммонизатора-гранулятора.
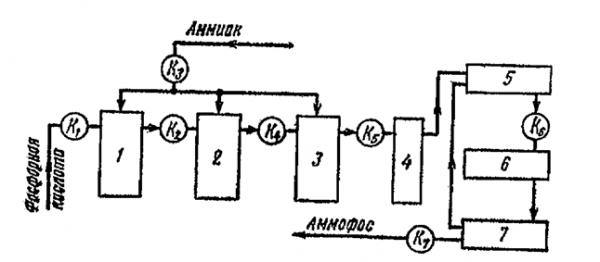
Рис.1. Основные точки контроля в производстве аммофоса:
1 — 3 — реакторы-сатураторы; 4 — промежуточные емкости; 5 — аммонизатор-гранулятор; 6 -барабанная сушилка; 7 — двухситный грохот; К1 — К7 — точки контроля;
Процесс начинается с каскада реакторов-сатураторов 1,2 и 3. Упаренная фосфорная кислота, содержащая 47-48% Р 2 О5, поступает в первый сатуратор, и в точке К1 в ней определяется содержанеи Р2 О5 . Аммиак, в жидком или газообразном состоянии, вводится в сатураторы 1 и 2 на расчетах нейтрализации кислоты на 80%, а в третий из расчетов образования 10-20% диаммонийфосфата. Концентрация аммиака контролируется в точке К3. В результате процесса нейтрализации пульпа нагревается до 115-1250 С. В точках К2 , К4 и К5 определяют-ся значения рН.
Пульпа из каскада реакторов-сатураторов поступает в промежуточную емкость 4, откуда насосом подается в аммонийзатор-гранулятор 5, где она смешивается с ретуром, масса которого в четыре раза превышает массу готового продукта. Влага поддерживается в пределах 2,5-3,5% и контролируется в точке К 6 . Средняя фракция после охлаждения идет на расфасовку, а крупная после измельчения и мелкая возвращается в смеситель-гранулятор как ретур. В точке К7 готовый продукт проверяют по ГОСТ.
В производстве аммофоса, как при производстве других сложных удобрении, особое значение имеет поддерживание заданного значения рН. На рисунке 2 представлена схема автоматического регулирования процесса нейтрализации в производстве аммофоса, основанная на поддержании заданного значения рН. По данной схеме нейтрализацию фосфорной кислоты аммиаком проводят в двух реакторах-сатураторах Р 1 и Р2 . На регуляторы соотношения потоков 5 воздействуют сигналы от блока умножения 2, преобразующего сигналы от расходомера 3 и от анализатора концентрации 1 (по плотности), расходомера аммиака 7 и одного из задатчиков 4. На задатчики поступают корректирующие сигналы от измерительных устройств 9 рН-метров 8. Под воздействием всех этих сигналов регуляторы соотношении потоков увеличиваю или уменьшают подачу аммиака с помощью регулирующих клапанов 6. Точность регулировании можно довести до рН+0,01. Если в реактор-сатуратор Р2 подавать более разбавленный раствор аммиака, тогда первый контур регулирования в реакторе Р1 будет осуществлять грубую компенсацию возмущений, а второй в реакторе Р2 более тонкую.
Аммофос, вследствие относительно высокого соедержания по отношению к азоту (отношение N: Р 2 О5 от 1:4,2 до 1:5,2) и отсутствия в своем составе калия, ограниченно применим как непосредственное удобрение. Более уравновешенные по содержанию азота, фосфора и калия сложные удобрения разных марок получают на основе фосфатов аммония добавлением азотного компонента-нитрата аммония и калийного компонента — хлорида или сульфата калия. Получаемые такм путем тройные сложные удобрения называются нитроаммофоска, двойные азотно-фосфорные, — нитроаммофос.Осваивается производство сложных удобрении на основе фосфатов аммония с добавлением азотного удобрения — карбамида. Они называются карбоамофоска и карбоаммофос.
Раздел 3. Расчетная часть
3.1Расчет материального баланса
Составить материальный баланс сатуратора для нейтрализации кислоты в производстве аммофоса (на 5000 кг фосфорной кислоты).
Состав экстракиционной фосфорной кислоты: 25% Р 2 О5 , 3,75% SO3 , 3,6% MgO, 0,2% CaO, 1,3% Al2 O3 , 1,3% Fe2 O3 , 1,86% F. Состав жидкого аммиака: 99% NН3 , 1% Н2 О. В процессе насыщения кислоты аммиаком испаряется 390 кг воды на 5000 кг кислоты. Содержание аммиака в нейтрализованной пульпе 27% от общего количества Р2 О5 .
Решение.
П р и х о д
В приходные статьи баланса включается фосфорная кислота и аммиак.
В 5000 кг фосфорной кислоты (25% Р 2 О5 ) содержиться, кг:
5000∙0,25∙2∙98
Н3 РО4 = 1725,35
142
Н 2 О 5000 — 1725,35 = 3274,65
Количество расходуемого аммиака равно 27% от общего количества Р 2 О5 , т.е.:
5000∙0,25∙0,27 = 337,5кг
С аммиаком поступает воды: (337,5∙1)/99 = 3,4 кг.
Р а с х о д
В результате обработки фосфорной кислоты аммиаком образуется пульпа и испаряется некоторое количество воды. Состав образующейся массы определяет-ся взаймодействием кислоты с содержащейся в ней примесями и аммиаком. В основу расчета количеств получаемых солей берем следующие стехиометричес-кие соотношения:
MgO + Н 3 РО4 + 2Н2 О = MgНРО4 ∙ 3Н2 О
СаО + Н 3 РО4 + Н2 О = СаНРО4 ∙ 2Н2 О
Al 2 O3 + 2Н3 РО4 = 2AlРО4 + 3Н2 О
Fe 2 O3 + 2Н3 РО4 = 2 FeРО4 + 3Н2 О
2NН 3 + Н2 SiF = (NH4 )2 SiF6
2NН 3 + Н2 SO4 = (NH4 )2 SO4
NН 3 + Н3 РО4 = NH4 H2 РО4
2NН 3 + Н3 РО4 = (NH4 )2 HРО4
При нейтрализации раствора фосфорной кислоты аммиаком в отделении сатурации получаются следующие соли, кг:
5000·0,036·174
димагнийфосфат = 783
40
в том числе кристаллизационной воды —
5000·0,036·3·18
= 243
40
5000·0,036·142
в том числе Р 2 О5 = 319,5
40·2
[40, 174, 18, 142 — молекулярные массы MgO, MgНРО 4 ∙ 3Н2 О, Н2 О и Р2 О5 ]
5000·0,002·172
дикальцийфосфат = 30,7
56
в том числе кристаллизационной воды —
5000·0,002·2·18
= 64,3
56
5000∙0,002∙142
в том числе Р 2 О5 = 12,7
56·2
[56 и 172 — молекулярные массы СаО и СаНРО 4 ∙2Н2 О]
5000·0,013·2·122
фосфат аллюминия = 155,5
102
5000∙0,013∙142
в том числе Р 2 О5 = 90,5
102
[102 и 122 — молекулярные массы Al 2 O3 и AlРО4 ]
5000·0,013·2·207
фосфат железа = 168
160
5000∙0,013∙142
в том числе Р 2 О5 = 57,5
160
[160 и 207 — молекулярные массы Fe 2 O3 и FeРО4 ]
5000·0,0186·178
кремнийфосфат аллюминия = 145
6·19
5000∙0,0186∙2·17
в том числе NН 3 = 27,5
6·19
[178, 17 и 19 — молекулярные массы (NH 4 )2 SiF6 , NН3 и молеклярная масса фтора]
5000·0,0375·132
сульфат аммония = 309,4
80
5000∙0,0375∙2·17
в том числе NН 3 = 79,5
80
[132 и 80 — молекулярные массы (NH 4 )2 SO4 и SO3 ]
Количество Р 2 О5 , связанной по первым четырем стехиометрическим соотношениям:
319,5 + 12,5 + 90,5 + 57,5 = 480 кг
Остальное количество Р 2 О5 связывается с аммиаком, образуя фосфаты аммония. Количество Р2 О5 , нейтрализуемого аммиаком:
5000·0,25 — 480 = 770 кг
Содержание аммиака в нейтрализованной пульпе составляет 27% от общего количества Р 2 О5 . Израсходовано аммиака на образование кремнифторида и сульфата аммония:
27,5 + 79,5 = 107 кг
Следовательно, на образование фосфатов аммония пошло аммиака:
1250·0,27-107 = 230,5
Количество аммиака, необходимое для связывания всей Р 2 О5 (770 кг) в моноаммонийфосфат:
2·17·770
= 184,4 кг
142
Но при этом остается избыточного аммиака 230,5 — 184,4 = 46,1 кг, который идет на образование диаммонийфосфата. Его количество:
46,1·132
= 178,9 кг
2·17
Это количество требует моноаммонийфосфата
(178,9·115)/132 z ≈ 155,8
где 115 и 132 — молекулятные массы NH 4 HРО4 и (NH4 )2 HРО4
Так как из 770 кг Р 2 О5 могло образоваться мноаммонийнофосфата
(115·184,4)/17 = 1248
то после образования диаммонийфосфата остается моноаммонийфосфата:
1248 — 155,8 = 1092,2 кг
Выход сухих солей (с учетом кристаллизационной воды) составляет:
783 + 30,5 + 155,5 + 168 + 145 + 309,5 + 1092,2 + 178,9 = 2862,6 кг
в том числе воды кристаллизационной: 243 + 6,5 = 249,5 кг.
Выход сухих солей без кристаллизационной воды:
2862,6 — 249,5 = 2613 кг.
Приводим состав сухих с учетом кристаллизационной воды:
кг %
MgНРО 4 3Н2 О…………………………………783 27,35
СаНРО 4 ∙ 2Н2 О………………………………..30,5 1,07
AlРО 4 ………………………………………….. 155,5 5,43
FeРО 4 …………………………………………….. 168 5,87
(NH 4 )2 SiF6 ………………………………………. 145 5,07
(NH 4 )2 SO4 ……………………………………… 309,5 10,81
NH 4 H2 РО4 ……………………………………….178,9 6,24
(NH 4 )2 HРО4 ……………………………………1092,2 38,16
Всего . . . . . . . . . . . . . . . . . . 2862,6 100
В систему поступает материалов (фосфорной кислоты, аммиака и воды с ним):
5000 + 337,5 + 3,4 = 5340,9
В процессе сатурации из систем испаряется 390 кг воды на 5000 кг кислоты. Количество пульпы после испарения воды равно:
5341- 390 = 4951 кг
В конечной пульпе содержиться свободной воды:
4951 — 2862,6 = 2088,4
Всего воды в пульпе:
2088,4 + 249,5 ≈ 2338 кг
Процентное содержание общей влаги в пульпе:
(2338·100)/ 4951 = 47,2%
Составляем материальный баланс сатурации в производстве аммофоса (на 5000 кг фосфорной кислоты):
Приход кг % Расход кг %
25%-ная по Р 2 О5 экс- солевая масса пульпы 2862,5 53,6
тракционная кислота в персчете на в то числе
моногидрат (100% Н 3 РО4 )…………………..1725 32,30 MgНРО4 ·3Н2 О 783
вода с фосфорной кислотой……………… .3275 61,32 СаНРО 4 ∙ 2Н2 О 30,5
аммиак…………………………………………….. 337,5 6,32 AlРО 4 155,5
вода с аммиаком……………………………….. .3,5 0,06 FeРО 4 168
(NH 4 )2 SiF6 145
(NH 4 )2 SO4 309,5
NH 4 H2 РО4 178,5
(NH 4 )2 HРО4 1092,5
вода в пульпе (свобод-
ная)……………………….2088,5 39,1
водяной пар……………………390 7,3
Всего………………. 5341 100 Всего ……………..5341 100
3.2 Расчет теплового баланса
Ипользуя данные материального баланса, рассчитать тепловой баланс сатурации в производстве аммофоса на 5000 кг фосфорной кислоты указанного выше состава. Температуры: поступающей кислоты 60 0 С, аммиака -270 С, при давлении 152 кПа (1,5 атм), отходящей пульпы 1020 С.
Решение
П р и х о д т е п л о т ы
Выделение теплоты за счет реакции, кДж:
образования моноаммонийфосфата —
Н 3 РО4 + NH3 = NH4 H2 PO4 + 75 362 кДЖ
(184,5·73 392)/17 = 817 900
[184,5 — количество (в кг) вступившего в реакцию аммиака]
образования диаммонийфосфата из моноаммонийфосфата —
NH 4 H2 PO4 + NH3 = (NH4 )H2 PO4 + 96 296 кДж/кмоль
(46·96 296)/17 = 260 565
[46 — количество (в кг) аммиака, реагирующего с моноаммонийфосфатом]
Н 2 SO4 + NH3 = (NH4 )2 SO4 + 193 849 кДж/кмоль
(79,5·193 849)/(2·17) = 453 265
[79,5 — количество (в кг) аммиака, связываемого в сульфат]
Н 2 SiF6 + 2NH3 = (NH4 )2 SiF6 + 159 089 кДж/кмоль
(27,5·159 089)/(2·17) = 128 680
[27,5- количество (в кг) аммиака, вступившего в реакцию]
Всего за счет химических реакции ………………………..1 660 410
(В расчете не включены из-за их малости тепловые эффекты других реакции).
Теплота, вносимая кислотой и аммиаком:
5000·2 868·60 + (-117,2·67,5) = 820 845 кДж
где 5000 — количество фосфорной кислоты, кг;
2 868 — средняя удельная теплоемкость кислоты, кДж/(кг·К);
60 — температура кислоты, 0 С;
- 117,2 — энтальпия аммиака при -27 0 С и 152 кПа (1,5 атм), кДж/кг;
67,5 — количество аммиака, кг;
Всего поступает теплоты: 1 660 410 + 820 845 = 2 481 255кДж
Р а с х о д т е п л о т ы
Нагревание пульпы до 102 0 С:
5341·2 721·102 = 1 387 710 кДж
где 5341 — количество пульпы, кг;
2 721 — средняя удельная теплоемкость пульпы, кДж/(кг·К);
102 — температура пульпы, 0 С;
Теплопотери в окружающую среду принимаем равными 3% от общего количества подводимой теплоты:
2 481 255
- 0,03 = 74 437,65 кДж
Всего расходуется теплоты: 1 387 710 + 74 437,65 = 1 462 147,6 кДж
Избыток теплоты расходуется на испарение воды: 2 481 255 — 1 462 147,6 ≈ 1 019 108 кДж.
Количество испаряющейся воды составит:
1 019 108/2 253 = 452,3 кг
где 2 253 — скрытая теплота испарения воды при 102 0 С, кДж/кг.
Общий расход теплоты: 1 387 710 + 74 437,65 + 1 019 108 = 2 481 255 к Дж
Составляем тепловой баланс сатурации фосфорной кислоты аммиаком (на 5000 кг фосфорной кислоты):
Приход кДж % Расход кДж %
теплота реакций обра- на нагревание
зования: пульпы……………………1 387 710 35,93
NH 4 H2 РО4 …………..817 900 32,96 на испарение воды…..1 019 105 41,07
(NH 4 )2 HРО4 …………260 565 10,50 теплопотери………………74 440 3,00
(NH 4 )2 SO4 ……………453 265 18,17
(NH 4 )2 SiF6 …………..128 680 5,19
теплота, вносимая фосфорной
кислотой и аммиаком….820 845 33,08
Всего………………2 481 255 100 Всего……………….2 481 255 100
3.3 Расчет гранулятора-аммонизатора
Гранулятор-аммонизатор имеет длину L = 6 м и диаметр D = 4 м. Определить частоту вращения барабана и теоретическое время пребывания в нем материала, если степень заполнения гранулятора равна 0,2, а наклон его по отношению к горизонту составляет ά = 2 0 .
Решение.
Частоту вращения барабана выбирают такой, при которой обеспечивается передвижение массы частиц вверх по стенке цилиндра, а затем ссыпание его вниз. Для этого скорость вращения барабана не должна превышать критическую п кр , когда под влиянием центробежной силы частицы прижимаются к поверхности барабана и не ссыпаются вниз.
Критическая скорость вращения барабана в 1 минуту определяется в зависимости от его диаметра по следующей формуле:
п кр = 42,3/√D
В зависимости от свойств материала фактическая скорость вращения п ф составляет разную долю от п кр . Для гранулирования сложных удобрении п ф должна быть ~ 35% от п кр
42,3 42,3·0,35
п ф =
- 0,35 = = 7,4 об/мин
√D √4
Теоретическое время пребывания материала в грануляторе (τ т , мин) определяют по формуле:
mkL
τт =
D n tg ά
где m — коэффициент, зависящий от отношения жидких и твердых веществ в грануляторе и гранулометрического состава продукта;
k — коэффициент, зависящий от устройства барабана (L, D, ά).
При степени заполнения барабана β = 0,2 (по перерабатываемому материалу без учета ретура) примем m = 1,0 и k = 2,04
1,0·2,0·6 12
τт = = = 11,6 минут
7,4·4
- tg 2 7,4·4·0,035
На практике фактическое время пребывания материала в грануляторе в 1,3-1,8 раза больше вычисленного.
Раздел 5. Экологическая характеристика производства
При производстве минеральных удобрении особое значение имеет борьба с выбросами вредных веществ в атмосферу и водоемы.
На различных стадиях производств минеральных удобрении при проведе-нии ряда физико-химических и тепловых процессов в газовую фазу выделяются аммиак, оксиды азота, серы, углерода, фтористые соединения и т.п., с одной стороны представляющие собой ценные продукты, с другой — являющиеся источником загрязнении, а порой и отравления окружающей среды. Поэтому проблема улавливания, обезвреживания и утилизации ценных веществ, содержащихся в отходящих газах, сродни проблемам комплексного использования сырья и создания безотходных технологии.
Очистка от фтора.
В зависимости от содержания фтористых соединении и их свойства отходящие газы подразделяются на три группы:
1) чистые операционное отделение производства) — утилизируемые газы;
2) с примесями пыли или брызг(отделение сушки, реакционное отделение производства) — газы утилизируются после очистки от примесей;
3) загрязненные пылью, брызгами, парами кислот и другими примесями — нейтрализируемые газы;
Неутелизируемые газы характеризуются низким содержанием фтора (0,1-0,6 г/м 3 ), который улавливают вместе с другимим примесями и пылью, водой или щелочными растворами с целью очитски отходящих газов до предельно допустимой концентрации (ПДК).
Водная абсорбция фтористых соединении практически сводится к поглощению туманообразной Н 2 SiF6 (гексафторкремниевая кислота).
Физические Н2 SiF6 , степень ее выделения зависят от температуры и концентрации кислоты. Повышение температуры и концентрации приводит к образованию твердых отложений на внутренних поверхностях оборудовании.
Высокая степень абсорбции фтористых соединении достигается при условии промывки газа циркулирующим раствором Н 2 SiF6 , имеющим ту же температуру, что и газ. Это приводит к предовращению конденсации воды и образовнию тумана.
На стадии санитарной очистки газов от фтористых соединении используют абсорбцию 0,5-3% гидроксидом кальция (известковым молоком):
2НF + Са(ОН) 2 → СаF2 + 2Н2 О
SiF 4 + 2Са(ОН)2 → 2СаF2 + SiО2 + Н2 О
Очистка от аммиака и оксидов азота.
Переход аммиака и фтора в газовую фазу происходит в основном при сушке пульпы влажных гранул аммофоса. При этом значительному разложению подвергается только диаммонийфосфат, отличающийся низкой термической стойкостью. Выход аммиака в газовую фазу существенно преобладает над выходом фтористых соединении. Естественно, при выборе системы очистки отходящих газов необходимо учитывать условия абсорбции как аммиака, так и фтористых соединении. Оксиды азота выделяются в газовую фазу при азотнокислом разложении фосфатов. В газовой фазе оксиды азота присутствуют обычно в виде NO, NO 2 , N2 O3 и N2 O4, причемNO не реагирует с водой, поэтому до абсорбции ему необходимо окислиться по реакции: 2NO + О2 = 2 NO2 .Монооксид азота NO может также соединеняться с диоксидом NO2 с образованием N2 O3 , который при абсорции водой дает чистую азотную кислоту. Однако N2 O3 присутствует в газах в заметных количествах лишь при низких температурах и высоких давлениях, поэтому его содержанием обычно принебрегают.
В качестве поглотителя аммиака, как правило применяют воду (вследствие его высокой растворимости в воде).
При поглощении аммиака водой получается аммиачная вода, концентрация которой зависит от содержания аммиака в очищаемых газах и от темепературы абсорбции. Аммиачная вода может быть использована напосредственно в качестве целевого продукта, но при этом она долна содержать 20-25% NН 3 ; при более низкой концентрации ее обычно используют в технологическом процессе.
При необходимости возвращения улавливаемого аммиака в процесс его иногда абсорбируют серной или фосфорной кислотой:
NН 3 + Н3 РО4 = NН4 Н2 РО4 , 2NН3 + Н2 SО4 = (NН4 )2 SО4,
Для концентрирования растворов фосфатов (или сульфатов) аммония с целью их возвращения в производство организуют рециркуляцию орошающих растворов.
Водная абсорбция диоксида азота (или N 2 O4 ) протекает по суммарной реакции:
3NO 2 + Н2 О = 2НNO3 , или 3N2 O4 + 2Н2 О = 4НNO3 + 2NO
При этом поглощается лишь 2 /3 введенного с NO2 азота, остальное количество поглощения должен быть окислен в газовой фазе. Таким образом, процесс абсорбции оксидов азота можно рассматривать как ряд последовательных стадии окисления и поглощегия.
Улавливание оксидов азота из отходящих газов проводят также растворами карбоната натрия (соды) или гидрооксида натрия (едкого натра), например:
Na 2 CO3 + NO + NO2 → NaNO3 + CO2 ,
Na 2 CO3 + 2NO2 →NaNO3 + CO2,
Образующийся растворы обрабатывают азотной кислотой для превращения нитрита натрия в нитрат, а затем путем выпаривания и кристаллизации извлекают из него нитрат натрия.
Очистка сточных вод.
Раздел 6. Охрана труда, техника безопасноти и противопожарная защита.
Вредными веществами в производстве комплексных удобрении являются неорганические кислоты, аммиак, пыль фосфата и готовых продуктов, фторосодержащие газы, оксиды азота.
Аммиак вызывает раздражение и ожоги слизистых облочек, дыхательных путей, кожного покрова. Предельно допустимая концентрация аммиака в воздухе производственных помешении 20 мг/м 3 . Аммиак образует с воздухом взрывоопасные смеси. Предельные взрывооасные концентрации аммиака в воздухе 15-27%.
Опасность представляет также аммиачная вода. Поскольку из аммиачной воды испаряется аммиак, для ее перевозки необходимы герметичные стальные или чугунные резервуары с предохранительными клапанами. Степень заполнения емкостей аммиачной водой должна быть не более 93%, так как при повышении температуры может сильно возрасти давление. После опорожнения цистерн в них остается взрывоопасная аммиачно-воздушная смесь. Поэтому при обслуживании и ремонте емкостей из-под аммиачной воды нужно соблюдать те же меры предосторожности, что и при обслуживании тары после легко воспламеняющихся жидкостей. При загорании аммиак можно тушить водой.
Для производства минеральных удобрении характерны многочиленные опреации, связанные с возможным выделением пыли: транспортирование, измельчение, рассев, сушка, охлаждение, кондиционирование, упаковка сыпучих материалов и продуктов. Для снижения засыпленности рабочих мест пылящее оборудование (размольные устройства, грохоты, транспортеры и др.) должны быть закрыты и иметь вентиляционные отсосы.
Во многих производствах минеральных удобрении применяются концентрированные кислоты — серная, азотная, фосфорная и др. Поэтому имеется опасность ожогов. Для предотвращения их следует работать в спецодежде. При разбавлении башенной или отработанной серной кислоты следует помнить о возможности выделения окислов азота, сернистого ангидрида или паров органических веществ (в зависимости от содержания примесей в отработанной кислоте).
В производстве минеральных удобрении опасность представляют многочисленные движущиеся механизмы, электрическое и механическое оборудование — насосы, компрессоры, фильтры, центрифуги, грохоты, размольные устройства, многочисленные транспортирующие устройства (транспортеры, элеваторы, шнеки) и др. Безопасная эксплуатация такого оборудования обеспечивается исправными ограждениями всех движущиеся частей. Для безопасного обслуживания шнеков, транспортеров и элеваторов запрещается на ходу производить их смазку, ремонт, а также надевать приводные ремни и натягивать транспортерные ленты. Чистку механического оборудования разрешается производить только после его остановки и снятия напряжения с электродвигателей. Преставляют опасность также аппараты, работающие под давлением и электрооборудование высокого напряжения.
При производстве комплексных удобрении необходимо соблюдать общие требования безопасности: работать в спецодежде, не принимать пищу, не пить и не курить на рабочем месте, принимать горячий душ после работы. Основными условием безопасной работы является тщательная герметизация оборудования и коммуникации, исправность вентиляционных устройств.
Основным условием безопасной эксплуатации производства является строгое соблюдение регламента и инструкции, исправность оборудования, хорошо работающая вентиляция, обеспечивающая допустимое содержание вредных веществ и пыли (что особенно важно для отделений, в которых возможны значительные выделения газов и пыли), нормальную температуру и влажность воздуха в отделениях с повышенным выделением влаги. Должны быть механизированны также трудоемкие процессы, как затаривание, взвешивание и зашивание мешков, транспортирование их на склад, погрузка готовой продукции в вагоны, подача топлива в топки сушильных барабанов, удаление золы и др.
Литература:
[Электронный ресурс]//URL: https://inzhpro.ru/kursovaya/proizvodstvo-kompleksnyih-udobreniy/
- «Основные процессы технологии минеральных удобрении» — П.В.Классен, И.Г.Гришаев, Москва «Химия» 1990;
- «Расчеты по технологии неорганических веществ» — М.Е.Прзин,
«Химия», 1977;
