Растворы — жидкая лекарственная форма, полученная растворением жидких, твердых или газообразных веществ в соответствующем растворителе. По дисперсологической классификации растворы — свободнодисперсные системы с жидкой дисперсионной средой.
В фармацевтической практике на долю растворов приходится в среднем до 30% общей рецептуры аптек. Большой удельный вес растворов, как и всех жидких лекарственных форм, объясняется рядом их преимуществ перед другими лекарственными формами.
Преимущества растворов в сравнении с твердыми лекарственными формами:
- высокая биодоступность;
- снижение раздражающих свойств;
- быстрое наступление терапевтического эффекта;
- возможность коррекции вкуса;
- простота и удобство применения.
Недостатки растворов в сравнении с твердыми лекарственными формами:
- непродолжительный срок хранения;
- необходимость разработки состава вспомогательных веществ. Присущие растворам недостатки не влияют на их широкое применение.
В зависимости от применяемого растворителя растворы выделяют водные и неводные растворы.
Растворы лекарственных веществ в неводных растворителях (растворы неводные) — жидкие лекарственные формы, представляющие собой гомогенные дисперсные системы, структурными единицами в которых являются ионы и молекулы.
Применение неводных растворов обусловлено тем, что многие лекарственные вещества не растворяются в воде. Неводные растворы обычно предназначены для наружного применения: смазывания слизистых оболочек, обтираний кожных покровов, примочек, ингаляций, полосканий, промываний, капель для носа и уха. Значительно реже они применяются внутрь и для ингаляций.
В соответствии с Приказом Министерства здравоохранения Российской Федерации от 16.07.97 г. N 214 все лекарственные средства, изготовленные в аптеках (в том числе гомеопатических) по индивидуальным рецептам или требованиям лечебных организаций, в виде внутриаптечной заготовки, фасовки, а также концентраты и полуфабрикаты подвергаются внутриаптечному контролю: письменному, органолептическому и контролю при отпуске — обязательно; опросному и физическому — выборочно.
Вспомогательные вещества в технологии лекарственных форм
... распределение суспендированных лекарственных веществ в тритурационных мазях, в расплавленных суппозиторных основ; уменьшается хрупкость таких основ. В то же время эти вспомогательные вещества могут оказывать выраженное влияние на такие важные характеристики лекарственных форм, как ...
Цель работы — изучить анализ неводных растворов.
1. Теоретическое исследование проблемы анализа неводных растворов
1 Характеристика неводных растворов
Неводные растворы классифицируют по их применению в медицинской практике:
- для внутреннего применения. В качестве растворителя относительно безопасно использование спирта, глицерина и пропиленгликоля для растворов антигистаминов, барбитуратов и витаминов. Однако пропиленгликоль обладает токсичным эффектом, особенно при применении в педиатрической практике;
- для наружного применения. С этой целью используют смеси спирта, димексида с хлороформом, глицерином, ацетоном и эфиром, жирными маслами.
Требования, предъявляемые к неводным растворам:
- соответствие медицинскому назначению для достижения необходимого лечебного эффекта;
- полнота растворения лекарственных веществ;
- отсутствие механических включений;
- стабильность при хранении.
Особенностью технологии растворов на нелетучих растворителях является применение растворителя с наилучшей растворяющей способностью для данного вещества (табл. 1).
Последовательность технологических операций такая же. как и в случае изготовления неводных растворов. за исключением того. что растворители загружают в порядке возрастания их вязкости или плотности (табл. 2).
Таблица 1
Растворимость некоторых лекарственных средств
|
Наименование вещества |
Растворимость 1,0 вещества в г растворителя |
||
|
глицерин |
масло |
спирт |
|
|
Йод |
1-200 |
1-10 |
1:10 |
|
Камфора |
1:840 |
10-30 |
1:1 |
|
Кислота борная |
7.0 при нагревании |
— |
25 (90%) 25 (70% медл.) |
|
Кислота салициловая |
1:62 |
1:8 касторовое 1:44 оливковое |
3 (90 %) 5.5 (70% медл.) |
|
Левомицетин |
1:50 при нагревании |
— |
1-10 (95%) 7 (70% медл.) |
|
Ментол |
— |
1-5 |
— |
|
Натрия гидрокарбонат |
4.0 |
— |
|
|
Натрия тетраборат |
1.5 |
— |
— |
|
Фенол |
1-10 |
1-10 |
|
Таблица 2
Плотность некоторых растворителей
|
Наименование |
Плотность, г/см 3 |
|
Глицерин |
1.225-1.235 |
|
Масло анисовое |
0.978-0.990 |
|
Масло вазелиновое |
0.875-0.890 |
|
Масло касторовое |
0.948-0.968 |
|
Масло миндальное |
0.913-0.918 |
|
Масло мятное |
0.900-0.910 |
|
Масло персиковое |
0.914-0.920 |
|
Масло подсолнечное |
0.921-0.926 |
|
Масло эвкалиптовое |
0.910-0.930 |
|
Скипидар |
0.855-0.860 |
|
Хлороформ |
1.474-1.483 |
неводный раствор лекарственный
Изготовление растворов в нелетучих растворителях проводят по массе. Масса таких растворов равна сумме масс ингредиентов. Растворение проходит медленно, поэтому целесообразно нагревание и перемешивание проводить непосредственно во флаконе для отпуска. Фильтрование — только при необходимости. желательно горячее. При охлаждении возможно образование осадка.
2 Растворители, применяемые для изготовления неводных растворов
Существует 3 класса растворителей для изготовления неводных растворов:
- летучие: этанол;
- эфир;
- хлороформ;
- нелетучие: глицерин;
- масла жирные;
- масло вазелиновое;
- димексид;
- полиэтиленоксид-400 (ПЭО-400);
- силиконы;
- комбинированные: сочетание этанола с глицерином, димексидом, водой.
Спирт этиловый (Spiritus aethylicus 95% и Spiritus aethylicus 90, 70 et 40%).
Растворяющая способность этанола зависит от его концентрации. Этанол легко смешивается с водой, глицерином, эфиром, хлороформом, ацетоном; обладает бактериостатическими и бактерицидными свойствами. В 95% этаноле легко растворяются неполярные вещества: органические кислоты, масла эфирные и жирные, камфора, ментол, йод, танин, левомицетин и др. В 40% спирте растворяются полярные вещества и некоторые соли.
Хлороформ (Chloroformium) — трихлорметан. В хлороформе хорошо растворяются лекарственные вещества, нерастворимые или малорастворимые в воде: кислота бензойная, бутадион, камфора, левомицетин, хлорбутанолгидрат, ментол и др. Хлороформ обладает токсическими, наркотическими и дезинфицирующими свойствами, относится к сильнодействующим веществам. Используют в мазях и линементах. Дозируют по массе.
Эфир медицинский (Aether medicinalis) — эфир диэтиловый. В технологии готовых лекарственных средств эфир находит применение при изготовлении некоторых настоек и экстрактов, а также в производстве коллодия. Последний представляет собой спиртоэфирный раствор коллоксилина. Дозируют по массе.
Глицерин (Glycerinum).
В фармацевтической практике применяют не абсолютный глицерин, а 86-90% водный раствор с относительной плотностью 1,224-1,235.
При разведении расчеты проводят по формуле:
= x. (a / b).
(b -1) / (а — 1),
где m — количество глицерина дистиллированного, г; х — количество глицерина разведенного, г; а — плотность глицерина дистиллированного, г/мл; b — плотность глицерина разведенного, г/мл; 1 — плотность воды.
Количество воды для разведения глицерина находят по разности:
у = х — m,
где у — количество воды, мл.
В глицерине легко растворяются: кислота борная, натрия тетраборат, хлоралгидрат, натрия гидрокарбонат и др. Растворы глицерина в концентрации 25% и выше не подвергаются микробной контаминации, более разбавленные растворы являются хорошей питательной средой для микроорганизмов. Ввиду высокой гигроскопичности глицерин хранят в хорошо укупоренных емкостях.
Масла жирные (Olea pinguid) — смесь глицеридов высших жирных кислот. Получают прессованием из семян и плодов. В аптечной практике используют масла: миндальное (Oleum Amygdalarum), персиковое (Oleum Persicorum), абрикосовое (Oleum Armeniacae), оливковое (Oleum Olivarum), подсолнечное (Oleum Helianthi).
Качество этих масел регламентируется в ГФ определенными показателями: величиной относительной плотности, кислотным числом, числом омыления, йодным числом и др.
Применяются в качестве растворителей неполярных и малополярных лекарственных веществ: камфоры, ментола, кислоты бензойной, фенола, тимола, некоторых витаминов. Кроме того, масла растительные находят применение в технологии линиментов, мазей, а также некоторых инъекционных растворов.
Масло вазелиновое — парафин жидкий (Oleum Vaselini, Paraffinum liquidum) — продукт переработки нефти, представляет собой смесь предельных углеводородов. Масло вазелиновое не всасывается через кожу и слизистые оболочки и замедляет резорбцию лекарственных веществ.
Существенным недостатком масла вазелинового является то, что при нанесении на кожу оно в значительной мере препятствует ее газо- и теплообмену, что при воспалительных процессах нежелательно. Применяют в составе мазей в сочетании с парафином.
Димексид (Dimexidum) — диметилсульфоксид (S0-(СН 3 )2 ).
Очень гигроскопичен. Хорошо смешивается с этанолом, ацетоном, глицерином, хлороформом, эфиром, маслом касторовым.
В димексиде легко растворяются лекарственные вещества различной химической природы. Проникает через неповрежденные ткани, проводя с собой лекарственные вещества (чрескожное введение).
Оказывает обезболивающее, противовоспалительное и жаропонижающее действие, а также обладает антимикробной активностью.
Полиэтиленгликоль-400 (Polyaethylenoxydum-400) (ПЭГ-400).
Структурная формула НОСН 2 (СН2 ОСН2 )тСН2 ОН. Бесцветная, подвижная жидкость с плотностью 1,14-1,16 г/см3 , температура кипения 238 ?С, смешивается с водой во всех соотношениях, растворим в ацетоне, спирте, глицерине, нерастворим в эфире, минеральных и жирных маслах. Соответственно, несовместим с перечисленными наполнителями, а также с антибиотиками, в частности с бацитрацином. Полиэтиленгликоль растворяется в поливинилхлориде, полиэтилене. Поэтому лекарственные формы, его содержащие, расфасовывают только во флаконы из стекла. В ПЭГ хорошо растворяются лекарственные вещества, содержащие гидроксильные группы: фенол, кислоты бензойная и салициловая, анестезин, камфора, фурацилин и др.
Эсилон-4 и эсилон-5 (Aesilonum) ((С 2 Н5 )2 Si-О-).
По свойствам близки к парафинам. Силиконовые жидкости используются в качестве защитных средств для кожи. За рубежом широко применяются в форме примочек, лосьонов, кремов и т.д.
3 Спирт этиловый
Спирт этиловый 95% С 2 Н5 ОН aethylicus 95%
Спирт этиловый может быть получен из природных соединений и синтетически.
В первом случае он получается брожением сахаристых веществ- полисахариды под влиянием ферментов превращаются в сахар мальтозу (I), которая в свою очередь расщепляется до глюкозы (II).
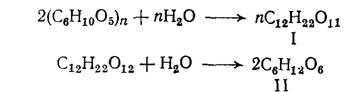
Конечным продуктом брожения глюкозы является спирт.
![]()
Этиловый спирт может быть получен синтетически из непредельных соединений:
- из этилена, при действии на него серной кислоты;
- последняя присоединяется к этилену, образуя серноэтиловый эфир, который при действии воды расщепляется на спирт и серную кислоту.
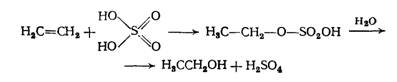
из ацетилена по реакции Кучерова; способ заключается в каталитическом гидрировании уксусного альдегида, который в свою очередь получается из ацетилена.
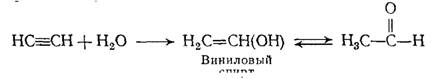
Уксусный альдегид отгоняется и восстанавливается водородом в присутствии катализатора (никель, сульфат ртути и др.)» при этом получается этиловый спирт.
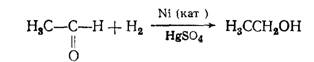
ГФ X описывает следующие препараты этилового спирта: спирт этиловый 95%; 90%; 70%; 40%.
Этиловый спирт — прозрачная жидкость. Он летуч, легко воспламеняется, имеет характерный запах, жгучий вкус; горит синеватым, слабо светящимся пламенем, смешивается во всех отношениях с водой, эфиром, хлороформом, ацетоном и глицерином.
Подлинность спирта устанавливается
а) образование йодоформа при взаимодействии с раствором йода в щелочной среде.
Реакция чувствительная, но недостаточно специфичная для спирта, ее дают соединения, имеющие в молекуле этоксильную (ОС 2 Н5 ), ацетогруппу (СН3 -С-) и оксиэтильную группу, например ацетон, молочная кислота и др.
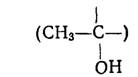
б) реакция образования сложных эфиров с кислотами; при взаимодействии спирта с ледяной уксусной кислотой в присутствии концентрированной серной кислоты образуется уксусно-этиловый эфир, обладающий своеобразным запахом.
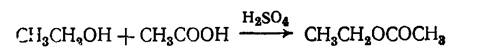
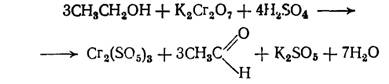
в) окисление спирта бихроматом калия в присутствии серной кислоты с образованием уксусного альдегида, имеющего запах свежих яблок.
Характерным показателем для спирта является величина плотности. В зависимости от концентрации спирта величина плотности различна. Чем меньше концентрация спирта, тем величина плотности больше. В ГФ X приводятся таблицы зависимости плотности от концентрации спирта.
В качестве примесей в этиловом спирте могут быть: продукты его окисления (ацетальдегид и уксусная кислота); продукты дегидратации (непредельные соединения, обладающие восстанавливающей способностью); остатки продуктов сырья и полупродуктов синтеза. Например, если этиловый спирт был получен брожением сахаристых веществ, в нем может быть примесь сивушных масел (смесь высших спиртов — бутилового-и изоамилового), которые определяют по неприятному запаху.
В «гидролизном спирте», полученном из древесных опилок, может быть примесь метилового спирта. Эта примесь недопустима, так как метиловый спирт очень ядовит и в определенной концентрации может привести к тяжелому отравлению и слепоте. В качестве примеси в спирте могут быть дубильные вещества, если спирт хранился в дубовых бочках.
Учитывая возможность наличия в спирте приведенных примесей, ГФ X предъявляет определенные требования к чистоте этилового спирта, применяющегося для медицинских целей. Так, нормируется предел кислотности спирта, предлагается проводить реакции обнаружения альдегидов с аммиачным раствором нитрата серебра, восстанавливающих веществ — с раствором перманганата калия, который не должен обесцвечиваться в течение 20 мин.
Дубильные вещества рекомендуется определять добавлением к пробе спирта небольшого количества раствора аммиака, при этом не должно появляться окрашивания. И обязательно требуется проведение реакции обнаружения примеси метилового спирта. Для этой цели используется общая реакция на спирты- окисление перманганата калия в кислой среде. В этом случае окисляется как сам этиловый спирт, так и примесь метилового спирта.
При окислении метилового спирта образуется формальдегид.
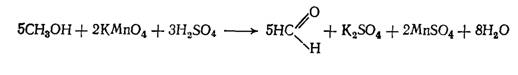
Формальдегид легко конденсируется с фенолами и, в частности, с фенолокислотой (хромотроповой) с образованием продукта конденсации фиолетового цвета. Ацетальдегид, образующийся при окислении этилового спирта, этой реакции не дает, так как способность к реакции конденсации у него очень мала.
По фармакологическим свойствам этиловый спирт относится к веществам наркотического действия. Воздействуя на кору головного мозга, он вызывает характерное алкогольное возбуждение, в больших дозах — ослабление возбудительных процессов коры и угнетение деятельности дыхательного центра.
При концентрациях 50-70% спирт обладает хорошими дезинфицирующими свойствами и применяется для дезинфекции рук и хирургических инструментов.
В медицинской практике спирт применяют обычно как наружное антисептическое и раздражающее средство для обтираний и компрессов. Этиловый спирт в различных разведениях применяется для изготовления настоек, экстрактов и ряда лекарственных форм, применяемых наружно. Спирт, кроме того, широко применяется в химической практике как растворитель. Спирт служит основным сырьем ряда химических производств,- из спирта получают уксус, хлороформ, йодоформ, различные эфиры и т.д.
Хранить следует в хорошо закупоренных стеклянных бутылях в прохладном месте.
Заключение
Неводными называют растворы, в которых растворителем служат органические вещества — спирты, эфиры, бензол и др.
Обычно органические растворители употребляются для растворения органических жидких и твердых веществ, например, масел, жиров, смол и т. д., и реже — неорганических веществ, как, например, некоторых солей, щелочей и минеральных кислот.
В настоящее время органические растворители применяют в практике аналитической химии для так называемого неводного титрования. Известно, что многие неорганические вещества растворяются в органических растворителях. Для неводного титрования готовят растворы с нормальной.концентрацией подобно тому, как для обычного титрования. Естественно, что свойства растворов в органических растворителях, применяемых для аналитических целей, отличаются от свойств водных растворов, так как поведение неорганических веществ в растворах прямо зависит от примененного растворителя.
При приготовлении растворов в органических растворителях расчеты проводят в зависимости от назначения раствора. Если он нужен не для аналитических целей, концентрацию растворенного вещества можно выражать в процентах, в граммах на литр и в молях органического вещества, т. е. так же, как и для водных растворов.
Список литературы
[Электронный ресурс]//URL: https://inzhpro.ru/referat/nevodnyie-rastvoryi-osobennosti-ih-izgotovleniya/
- Государственная Фармакопея РФ, 10-е издание. — М.: Медицина, 1968. — 1079 с.
- Фармацевтическая технология: учеб.
пособие для студентов учреждений сред. проф. образования, обучающихся по специальности 060301.51 «Фармация» по дисциплине « Фармацевтическая технология»/ В.А. Гроссман. 2012-320с.
- Меленьбева Г.А. Фармацевтическая химия. — В.А. Гроссман. 2008. -320с.
