Термин «антибиотик» был предложен в 1942 г. С. А. Ваксманом для обозначения веществ, образуемых микроорганизмами и обладающих антимикробным действием. Впоследствии многие исследователи предлагали свои формулировки, вкладывая в них подчас слишком ограниченное содержание либо чрезмерно расширяя это понятие.
В настоящее время под антибиотиками понимают химиотерапевтические вещества, полученные из микроорганизмов или иных природных источников, а также их полусинтетические аналоги и производные, обладающие способностью избирательно подавлять в организме больного возбудителей заболеваний и (или) задерживать развитие злокачественных новообразований.
Антибиотики природного происхождения продуцируются различными группами микроорганизмов (чаще всего актиномицетами, реже бактериями), низшими растениями (дрожжами, водорослями, плесневыми грибами, высшими грибами), высшими растениями и животными организмами.
Например, представители родов Micrococcus, Streptococcus, Diplocoooccus, Chromobacterium, Escherichia, Proteus синтезируют низин, дипломицин, продигиозин, колиформин. Бактерии рода Bacillus образуют грамицидины, субтилин, полимиксины.
Антибиотики, образуемые микроорганизмами, принадлежащими к ряду Actinomycetales, — стрептомицин, тетрациклины, новобиоцин, актиномицины и др.
Антибиотики, образуемые несовершенными грибами: пенициллин — Penic. Chrysogenum; гризеофульвин — Penic. Griseofulnum; трихоцетин — Tricholecium roseum.
Антибиотики, образуемые грибами, относящимися к классам базидиомицетов и аскомицетов: термофиллин, лензитин, хетомин.
Лишайники, водоросли и низшие растения способны образовывать усниновую кислоту и хлореллин, высшие растения – алмицин, рафанин.
Антибиотики животного происхождения: лизоцим, экмолин, круцин, интерферон.
Классификация антибиотиков.
- бактериостатические (бактерии живы, но не в состоянии размножаться),
- бактерициды (бактерии умертвляются, но физически продолжают присутствовать в среде),
- бактериолитические (бактерии умертвляются, и бактериальные клеточные стенки разрушаются).
По механизму биологического действия антибиотики делятся:
1. Антибиотики, ингибирующие синтез бактериальной стенки (пенициллины, цефалоспорины, бацитрацин, ванкомицин).
2. Антибиотики, нарушающие функционирование цитоплазматической мембраны (полипептиды, полиены, грамицидин).
Производство антибиотиков
... в состав некоторых антибиотиков, образуемых грибами, бактериями и актиномицетами. Обычно источником серы в среде служат сульфаты. Однако при биосинтезе пенициллина лучшим источником серы ... штамма -- продуцента антибиотика, пригодного для промышленного производства; 2. биосинтез антибиотика; 3. выделение и очистка антибиотика; 4. концентрирование, стабилизация антибиотика и получение готового ...
3. Антибиотики, разрушающие рибосомальные субчастицы и сдерживающие синтез белка (тетрациклины, хлормицетины, аминогликозиды, макролиды).
4. Антибиотики, избирательно подавляющие синтез нуклеиновых кислот:
- ингибиторы синтеза РНК (актиномицин, гризеофульвин, канамицин, неомицин, новобиоцин и др.);
- ингибиторы синтеза ДНК (брунеомицин, саркомицин).
Антибиотики обладают избирательным действием, т.е. активны только в отношении микроорганизмов при сохранении жизнеспособности клеток хозяина и действуют не на все, а на определенные роды и виды микроорганизмов. С избирательностью тесно связано понятие о широте спектра активности антибиотиков. Традиционно по спектру антимикробного воздействия антибиотики делятся на препараты узкого спектра действия и широкого:
1. Антибиотики узкого спектра действия действуют только определенный вид бактерий. К ним относятся пенициллин, оксациллин, эритромицин.
2. Антибиотики с широким спектром действия эффективны в уничтожении не исключительно грамположительных и грамотрицательных бактерий, но также спирохет, лептоспир, риккетсий, крупных вирусов (трахомы, пситтакоза и других).
К ним относят группы тетрациклина (тетрациклин, окситетрациклин, хлортетрациклин, глициклин, метациклин, морфоциклин, доксициклин) и левомицетина.
Выражение величин биологической активности антибиотиков обычно производят в условных единицах, содержащихся в 1 мл раствора (ед/мл) или в 1 мг препарата (ед/мг).
За единицу антибиотической активности принимают минимальное количество антибиотика, способное подавить развитие или задержать рост стандартного штамма тест-микроба в определенном объеме питательной среды.
Применение антибиотиков.
В настоящее время ведутся активные работы по изысканию антибиотиков нового поколения, эффективных при лечении вирусных и раковых заболеваний.
Антибиотики находят применение в сельском хозяйстве, прежде всего как лечебные препараты в животноводстве, птицеводстве, пчеловодстве и растениеводстве, а отдельные антибиотические вещества — как стимуляторы роста животных.
Некоторые из антибиотиков с успехом применяются в пищевой и консервной промышленности в качестве консервантов скоропортящихся продуктов (свежей рыбы, мяса, сыра, различных овощей).
2. Особенности получения антибиотиков
Процесс получения антибиотика включает в себя следующие основные стадии (рис. 1):
1. получение соответствующего штамма — продуцента антибиотика, пригодного для промышленного производства;
2. биосинтез антибиотика;
3. выделение и очистка антибиотика;
4. концентрирование, стабилизация антибиотика и получение готового продукта.
Первая задача при поиске продуцентов антибиотиков — выделение их из природных источников. Биосинтез антибиотиков — наследственная особенность организмов, проявляющаяся в том, что каждый вид (штамм) способен образовывать один или несколько вполне определенных, строго специфичных для него антибиотических веществ.
Выявление потенциальной возможности образовывать в процессе жизнедеятельности антибиотики связано с условиями культивирования организмов. В одних условиях организм образует антибиотик, в других условиях тот же организм при хорошем росте не будет обладать способностью синтезировать антибиотическое вещество. Образование антибиотиков будет происходить только при развитии организма в специфической среде и при наличии особых внешних условий. Путем изменения условий культивирования можно получить больший или меньший выход антибиотика, или создать условия, при которых антибиотик вообще не будет образовываться. Можно также путем изменения условий культивирования продуцента добиться преимущественного биосинтеза одного из антибиотиков, при условии образования изучаемым организмом нескольких антибиотических веществ, или же получить новые формы антибиотиков, но только в пределах тех соединений, которые способны синтезироваться этим организмом.
Биотехнология антибиотиков
... 1) внедрение в производство наиболее высокопродуктивных штаммов микроорганизмов -- продуцентов антибиотиков; 2) создание и обеспечение самых благоприятных условий развития продуцента антибиотика на относительно дешевых средах; 3) широкое ... для небольших объемов с тем же эффектом стерилизации. Наилучший эффект стерилизации и сохранения термолабильных веществ среды получается в том случае, ...
К числу наиболее существенных факторов, оказывающих влияние на проявление антибиотических свойств микроорганизмов, относятся состав среды, ее активная кислотность, окислительно-восстановительные условия, температура культивирования, методы совместного выращивания двух или большего числа микроорганизмов и другие факторы.
Среды для культивирования микроорганизмов.
- мясопептонная среда, в состав которой одновременно с мясным экстрактом и пептоном входят хлорид натрия, фосфат калия, иногда глюкоза или сахароза;
- используется обычно в лабораторной практике.
- картофельные среды с глюкозой и пептоном, часто используемые в лаборатории для культивирования многих видов актиномицетов и бактерий;
- среды с кукурузным экстрактом, соевой мукой, бардой и другими веществами, в состав которых входят сульфат аммония, карбонат кальция, фосфаты, глюкоза, сахароза, лактоза или иные углеводы и ряд других соединений; среды успешно применяются в промышленности, т.
к. являются дешевыми и обеспечивают хорошее развитие микроорганизмов с высоким выходом антибиотиков.
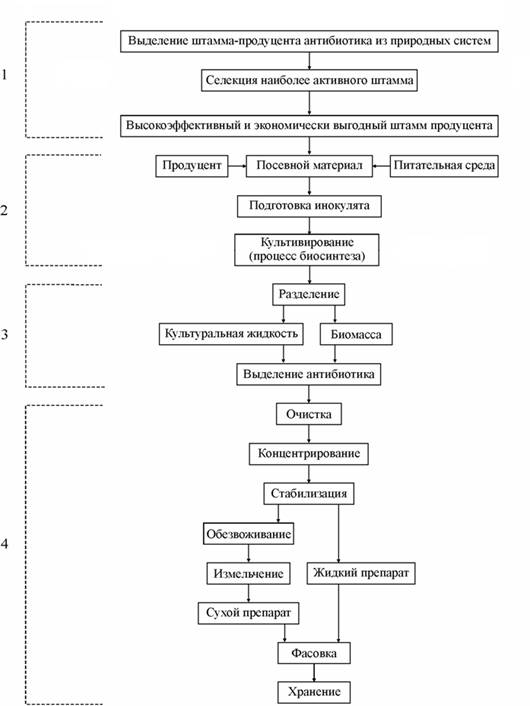
Рис. 1 — Схема производства антибиотиков в процессе микробного биосинтеза
Поскольку натуральные среды не позволяют получать строгие количественные данные для изучения физиологических и биохимических особенностей организма, применяют синтетические среды, которые подбирают для отдельных продуцентов индивидуально.
Источниками углерода могут быть органические кислоты, спирты, углеводы, сочетания различных углеродсодержащих соединений. При промышленном получении ряда антибиотиков в качестве источников углерода нередко применяют картофельный крахмал, кукурузную муку или другие растительные материалы.
Источники азота оказывают большое влияние на образование микроорганизмами антибиотических веществ. Обычно в средах для культивирования микроорганизмов источником азота служат соли азотной (реже азотистой) кислоты, аммонийные соли органических и неорганических кислот, аминокислоты, белки и продукты их гидролиза.
Обычно наиболее благоприятным для микроорганизмов является соотношение C/N = 20. Однако для образования антибиотика такое соотношение не всегда оптимально. Поэтому для каждого продуцента необходимо подбирать соответствующее соотношение углерода и азота.
Продуценты антибиотиков по отношению к концентрации фосфора в среде можно разделить на три группы:
- высокочувствительные продуценты, для которых оптимальная концентрация фосфора в среде составляет менее 0,01 % (продуценты нистатина, тетрациклинов, флоримицина, ванкомицина);
- продуценты средней чувствительности, для которых оптимальная концентрация фосфора составляет 0,010–0,015 % (продуценты стрептомицина, эритромицина, циклосерина, неомицина);
- малочувствительные продуценты, для которых оптимальная концентрация фосфора составляет 0,018–0,020 % (продуценты новобиоцина, грамицидина, олеандомицина).
9 стр., 4064 слов
Антибиотики в продуктах питания животного происхождения
... антибиотики, например пенициллин), полусинтетические (продукты модификации природных молекул, например, амоксициллин или цефазолин) и синтетические (например, сульфаниламиды, нитрофураны). Современная классификация антибиотиков разработана в Государственном центре по антибиотикам (С.М.Навашин, 1994), в соответствии ...
Сера входит в состав некоторых антибиотиков, образуемых грибами (пенициллин, цефалоспорин, глиотоксин и др.), бактериями (бацитрацины, субтилины, низины) и актиномицетами (эхиномицины, группа тиострептона).
Обычно источником серы в среде служат сульфаты. Однако при биосинтезе пенициллина лучшим источником серы для продуцента служит тиосульфат натрия.
Кроме того, для биосинтеза антибиотиков необходимы и отдельные микроэлементы. Так, продуцент альбомицина S. subtropicus образует антибиотик при значительной концентрации железа в среде. Железо необходимо для образования хлорамфеникола и других антибиотиков.
Биосинтезу ряда антибиотических веществ (хлорамфеникола, стрептомицина, пенициллина и др.) способствуют ионы цинка.
Стимулирующее влияние на биосинтез гентамицина, курамицина А, фософономицина оказывают ионы кобальта.
Ионы галогенов входят в состав некоторых тетрациклиновых антибиотиков и хлорамфеникола.
Влияние рН среды.
Большинство актиномицетов хорошо развиваются при начальных значениях рН среды в пределах от 6,7 до 7,8; в большинстве случаев жизнеспособность актиномицетов при рН ниже 4,0–4,5 подавлена.
Температура.
Актиномицеты, как правило, культивируются при температуре 26–30°С, хотя некоторые виды стрептомицетов могут развиваться как при пониженных (от 0 до 18 °С), так и при повышенных (55–60 °С) температурах.
Для большинства мицелиальных грибов оптимальная температура составляет 25–28 °С.
Аэрация. Большинство изученных продуцентов антибиотиков являются аэробами. Для биосинтеза многих антибиотиков (пенициллин, стрептомицин и др.) максимальное их накопление происходит при степени аэрации, равной единице, при которой через определенный объем среды за 1 мин продувается такой же объем воздуха.
В процессе развития продуцента антибиотика в промышленных условиях потребность организма в кислороде меняется в зависимости от стадии развития, вязкости культуральной жидкости и других факторов. На определенных стадиях могут возникнуть ситуации, связанные с кислородным голоданием продуцента. В этих условиях следует принимать дополнительные меры, например, повышение концентрации окислителя добавлением пероксида водорода.
Наиболее перспективным методом выращивания микроорганизмов — продуцентов антибиотиков признан метод глубинного культивирования с использованием периодических процессов. В условиях глубинной культуры процесс развития организма и синтеза антибиотика проходит в две фазы.
В первой фазе развития культуры или, как ее иногда называют, тропофазе (фаза сбалансированного роста микроорганизма), наблюдается интенсивное накопление биомассы продуцента, связанное с быстрым потреблением основных компонентов среды и с высоким уровнем поглощения кислорода.
Во второй фазе развития, именуемой идиофазой (фаза несбалансированного роста микроорганизма), накопление биомассы замедлено или даже уменьшено. В этот период продукты метаболизма микроорганизма лишь частично используются на построение клеточного материала, они в основном направляются на биосинтез антибиотика. Обычно максимум продукции антибиотика в среде наступает после максимума накопления биомассы. Подробное описание технологического процесса на примере производства пенициллина приведено в следующей главе.
3. Производство пенициллина
Пенициллин был открыт в 1929 г. Александром Флемингом и был выделен в кристаллическом виде 1940 году. Установлено, что пенициллин оказывает антимикробное действие в отношении некоторых грамположительных бактерий (стафиллококков, стрептококков, диплококков и некоторых других) и практически неактивен в отношении грамотрицательных видов и дрожжей.
Способность образовывать пенициллин широко распространена среди многих плесневых грибов, относящихся к родам Penicillium и Aspergillus. Однако это свойство более характерно для группы Penicillium notatum-chrysogenum. Первые выделенные из естественных субстратов штаммы как наиболее активные продуценты пенициллина образовывали не более 20 единиц (12 мкг) антибиотика на 1 мл культуральной жидкости. В результате широкой научной работы по селекции новых активных штаммов продуцентов пенициллина получены различные штаммы Penicilliumchrysogenum, которые, в отличие от исходных штаммов, обладают высокой продуктивностью и используются в промышленности. В настоящее время в промышленных условиях получают культуральные жидкости с содержанием пенициллина более 15000 ед/мл, а отдельные штаммы способны синтезировать антибиотик в количестве до 25 тыс. ед/мл.
Под названием «пенициллин» объединена обширная группа веществ, которые являются N-ацильными производными гетероциклической аминокислоты. Из природных пенициллинов применяются бензилпенициллин и феноксиметилпенициллин.
3.1 Технологическая схема производства пенициллина
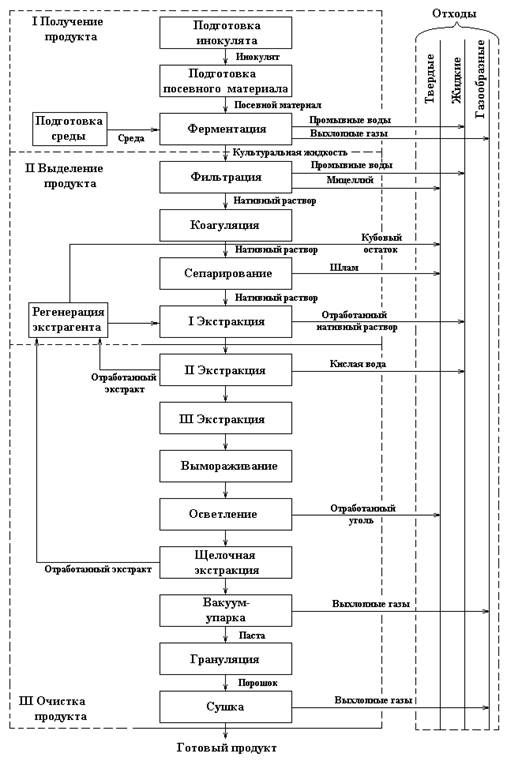
3.2 Изложение технологического процесса
3.2.1 Подготовка инокулята
Подготовка посевного материала включает следующие стадии:
1) выращивание посевного мицелия 1-й генерации в аппаратах малой емкости (инокуляторах);
2) выращивание посевного мицелия 2-й генерации в аппаратах большой емкости.
Споровая культура, используемая для засева инокулятора, выращивается на пшене в стеклянных флаконах, высушивается и в таком виде хранится при комнатной температуре. Засев производят сухими спорами из 2-3 флаконов.
Основной задачей при культивировании продуцента пенициллина в посевных аппаратах на стадии подготовки инокулята является быстрое получение большой массы мицелия, способного обеспечить при пересеве в ферментер интенсивный рост и высокий выход антибиотика. Для осуществления этой задачи продуцент необходимо выращивать на средах, богатых легкоусвояемыми питательными веществами, в условиях хорошей аэрации, при оптимальной для роста микроорганизма температуре.
В качестве легкоусвояемого углерода выступает глюкоза, сахароза и т.д. В качестве второго источника углерода применяют в небольших количествах лактозу, присутствие которой в среде для выращивания посевного мицелия желательно по следующей причине: ее потребление начинается не сразу, а после некоторого периода адаптации (привыкания), в течение которого происходит образование фермента, расщепляющего лактозу. Посевной мицелий, выращенный на среде, содержащей лактозу, обладает более высокой ферментативной активностью по отношению к трудноусвояемой лактозе и быстрее потребляет ее, что положительно сказывается на ходе ферментации.
Потребность гриба в азоте легко удовлетворяется минеральным азотом — аммонийным или нитратным. Помимо неорганического азота, в состав посевных сред, применяемых в промышленности, входит богатое органическим азотом растительное сырье типа кукурузного экстракта.Растительное сырье характеризуется не только наличием органического азота, оно содержит дополнительный углерод, входящий в состав аминокислот, полипептидов и белков, а также минеральные элементы, витамины и ростовые вещества.
Кроме углерода и азота, для роста микроорганизма необходимы фосфор, сера, магний, калий и микроэлементы – марганец, цинк, железо, медь. Большинство известных посевных сред содержит почти все вышеуказанные элементы, но в различных соотношениях. В таблице 1 приведен пример среды, применяемой для выращивания посевного материала.
Таблица 1 – Состав одной из сред для выращивания посевного материала.
| Вещество | % |
| Кукурузный экстракт | 2 (на сухой вес) |
| Глюкоза | 2 |
| Лактоза | 0,5 |
| Азотнокислый аммоний | 0,125 |
| Однозамещенный фосфорнокислый калий | 0,2 |
| Сернокислый магний | 0,025 |
| Сернокислый натрий | 0,05 |
| Мел | 0,5 |
Существенное влияние на рост мицелия оказывает рН среды. Наиболее благоприятное значение рН для роста мицелия лежит между 6,0-6,5. При более кислом или более щелочном рН рост и развитие микроорганизма замедляются.
Выращивание посевного мицелия продолжается 36-50 часов до получения биомассы средней густоты. Мицелий, выращенный в инокуляторах, передается в количестве 10% по объему в посевные аппараты, где культивируется в течение 12-18 часов, а затем передается в большие ферментеры в количестве 15-20%. Процесс выращивания посевного мицелия 1-й и 2-й генерации осуществляется при температуре 24-26°.
Пенициллы — продуценты пенициллина являются типичными аэробами и требуют для своего роста и развития наличия кислорода. Для получения высокопродуктивного посевного мицелия наряду с оптимальной питательной средой необходимо обеспечить и достаточное снабжение гриба. В процессе производства пенициллина выращивание посевного мицелия осуществляют при непрерывном перемешивании и бесперебойной подаче воздуха в аппараты в количестве 1,2-1,5 объема воздуха на 1 объем среды в минуту.
3.2.2 Процесс ферментации
Ферментация является основной стадией в производстве пенициллина, на которой формируется целевой продукт. В промышленности применяется метод глубинной ферментации, при котором культура микроорганизма выращивается в питательной среде, заполняя весь ее объем. У различных штаммов потребность в источниках питания неодинакова. В связи с этим состав сред не является постоянным и универсальным для всех продуцентов, образующих пенициллин, и меняется с появлением новых штаммов.
Ферментационная среда должна быть составлена таким образом, чтобы развивающаяся культура, потребляя питательные вещества и выделяя продукты обмена, сама создавала необходимые условия и осуществляла переход от фазы роста мицелия к фазе пенициллинообразования. Желательно, чтобы вторая фаза была более продолжительной и чтобы процесс ферментации прекращался до наступления автолиза.
Для этого, как и при выращивании посевного материала необходимо одновременное присутствие в среде как легко-, так и трудноусвояемого углевода. Легкоусвояемый углевод обеспечивает быстрый рост и образование обильной биомассы; трудноусвояемый углевод создает условия, благоприятные для биосинтеза антибиотика.
При промышленном биосинтезе пенициллина наибольшее распространение в качестве легкоусвояемого углевода получила глюкоза или гидрол. Трудноусвояемым углеводом является лактоза. Лактоза является единственным углеводом, обеспечивающим полноценное протекание фазы пенициллинообразования. Высокий выход антитибиотика получают только при наличии в среде лактозыв качестве основного источника углевода. Лактоза находится в культуральной жидкости на протяжении всего процесса ферментации, благодаря чему мицелий обеспечен сахаром, биомасса в течение пенициллинообразования медленно растет, и накопление антибиотика достигает максимального уровня.
В состав ферментационных сред входит органический и минеральный азот. Отличным источником органического азота считается кукурузный экстракт, но он может быть с успехом заменен пшеничным экстрактом, различными жмыхами, соевой мукой, глютеном и другим растительным сырьем, богатым азотом.
Исключительно важную роль в обмене веществ клетки играет фосфор, который необходим не только для нормального роста и развития гриба, но и для осуществления самого процесса биосинтеза пенициллина. Для образования пенициллина требуется значительно более высокая концентрация фосфора в среде, чем для роста гриба.
Обязательным компонентом ферментационной среды является сера, входящая в состав важнейших аминокислот и ферментов. Сера необходима еще и потому, что она входит в состав молекулы пенициллина. В питательные среды сера вносится в виде солей серной кислоты и гипосульфита.
Из других элементов, необходимых для нормальной жизнедеятельности гриба и образования антибиотика, следует отметить калий, магний, цинк, железо, марганец, медь.
Также необходимо присутствие предшественников в среде. Предшественниками называются вещества, непосредственно включающиеся в молекулу получаемого продукта. Предшественником бензилпенициллина является фенилуксусная кислота (ФУК) или ее производные — фенилацетамид (ФАА), фенилэтиламин, фенилацетилглицин и другие вещества. Предшественником феноксиметилпенициллина является феноксиуксусная кислота (ФОУК).
Оптимальная концентрация предшественника в среде устанавливается в зависимости от эффективности его использования для биосинтеза пенициллина данным штаммом.
Для биосинтеза пенициллина наиболее благоприятно нейтральное значение рН. Для поддержания в культуральной жидкости определенного уровня рН рекомендуется регулировать его с помощью автоматического добавления кислоты или щелочи либо путем установления правильного соотношения компонентов среды. В синтетических средах в качестве регуляторов рН чаще всего применяют органические кислоты, в комплексных средах — мел. Своеобразным регулятором рН при промышленном получении пенициллина является кашалотовый жир, который добавляется в среду в процессе ферментации как пеногаситель.
Для получения максимального выхода пенициллина основные компоненты среды должны входить в ее состав в строго определенных соотношениях и концентрациях. Состав некоторых сред, применяемых в производстве пенициллина представлен в таблице 2.
Таблица 2 – Состав сред, применяемых для получения пенициллина
| Компоненты | Среда | ||
| кукурузная | жмыховая | жировая | |
| Кукурузный экстракт | 2,0 – 3,0 | — | 2,0 – 3,0 |
| Жмыхи (арахисовый, подсолнечный, соевый и др.) | — | 2,0 – 4,0 | — |
| Лактоза | 5,0 | 5,0 | 1,0 |
| Глюкоза или гидрол | 1,5 | 1,5 | 1,5 |
| Кашалотовый жир или растительные масла | 0,5 – 0,1 | 0,5 – 0,1 | 2,5 – 3,5 |
| Азотнокислый аммоний | 0,4 | 0,4 | 0,4 |
| Сернокислый натрий | 0,05 | 0,05 | 0,05 |
| Фосфорнокислый калий однозамещенный | 0,4 | 0,4 | 0,4 |
| Сернокислый магний | 0,025 | 0,025 | 0,025 |
| Серноватистокислыый натрий (гипосульфит) | 0,2 | 0,2 | 0,2 |
| Мел | 0,5 – 1,0 | 0,5 – 1,0 | 0,5 – 1,0 |
| Предшественник | 0,3 – 0,4 | 0,3 – 0,4 | 0,3 – 0,4 |
Основными показателями, свидетельствующими об окончании ферментации, являются полное исчезновение углеводов в культуральной жидкости и прекращение биосинтеза антибиотика. Процесс ферментации в производственных условиях осуществляется при температуре 26±1 0 С и продолжается обычно 120-125 часов.
Интенсивность биосинтеза пенициллина зависит от количества мицелия, образуемого в процессе ферментации. Большая биомасса образует больше пенициллина, поэтому содержание углеводов, азота, фосфора и серы в среде должно быть достаточно высоким, чтобы обеспечить максимальное образование мицелия. Однако большая биомасса еще не гарантирует высокого выхода антибиотика. Гриб необходимо обеспечить не только достаточным количеством питательных веществ, но и необходимым количеством кислорода. Питание гриба и аэрация являются двумя сторонами одного процесса – чем больше питательных веществ в среде, тем больше требуется кислорода для их окисления. С другой стороны, повышение концентрации питательных веществ в среде ведет к увеличению биомассы, для дыхания которой требуется пропорционально большее количество кислорода. Состав питательной среды и аэрация взаимообусловлены. Максимальное количество пенициллина может быть получено только на средах с высокой концентрацией компонентов в условиях достаточного снабжения культуры растворенным кислородом.
Важным условием успешного проведения процесса биосинтеза пенициллина является строгое соблюдение условий асептики, так как попадание посторонних микроорганизмов может резко снизить выход антибиотика. Многие распространенные микроорганизмы способны образовывать фермент пенициллиназу, расщепляющий пенициллины. Попадание даже небольшого числа бактерий, способных вырабатывать пенициллиназу, приводит к полной инактивации пенициллина, в связи чемследует уделять особое внимание стерильности питательных сред, воздухаи вспомогательных материалов.
Необходимость обеспечения условий стерильности процессов при технологических связях агрегатов между собой коллекторными системами загрузки питательных сред, передачи посевного материала из инокуляторов в ферментаторы накладывает более высокие требования к уровню автоматизации этих процессов.
3.2.3 Фильтрация
Обычно для отделения мицелия от культуральной жидкости применяют вакуум-барабанные фильтры непрерывного действия. Фильтрацию начинают до начала автолиза мицелия, поскольку при фильтрации автолизированной культуры мицелий не образует плотной пленки на фильтрующей поверхности барабана, а налипает в виде отдельных тонких комков, которые сами не отходят в зоне «отдувки» фильтра, и их приходится удалять вручную. При этом продолжительность фильтрации увеличивается в 2 — 3 раза, выход фильтрата резко падает, а сам фильтрат получается очень мутным.
Необходимо тщательно соблюдать условия, препятствующие разрушению пенициллина во время фильтрации, — охлаждение нативного раствора до 4-6°С и систематическая (после каждой загрузки) обработка фильтра, коммуникаций и сборников антисептиками, например хлорамином. Фильтр также должен систематически стерилизоваться острым паром.
3.2.4 Предварительная обработка нативного раствора
Нативный раствор (фильтрат культуральной жидкости) представляет собой более или менее мутную, окрашенную в желто-коричневый или зеленовато-коричневый цвет жидкость. Величина рН среды в зависимости от штамма продуцента, состава среды и продолжительности процесса ферментации обычно колеблется от 6,2 до 8,2.
Очень важной характеристикой нативного раствора является содержание в нем белковых веществ, определяемых осаждением трихлоруксусной кислотой или другим соответствующим методом.
Применяется несколько способов предварительной обработки нативного раствора с целью освобождения от белковых примесей: осаждение солями многовалентных металлов (например, А1 3+ Fе3+ или Zn2+ ), коагуляция танином, термическая коагуляция при температуре 60-75°С и рН 5,5 — 6,0, осаждение примесей катионными детергентами типа четвертичных аммониевых оснований (например, цетилпиридиний-бромидом или додецилтриметиламмонийхлоридом и т.п.).
Применение этих методов приводит к потерям антибиотика. Обычно в результате коагуляции и последующей фильтрации или сепарирования теряется от 5 до 15%) пенициллина. При этом коагуляция солями металлов позволяет удалять не более 50% общего количества белковых веществ.
3.2.5 Экстракция и очистка пенициллина
Нативный раствор содержит 3-6% сухих веществ. На минеральные вещества приходится 30-40% сухого остатка, от 15 до 30% приходится на пенициллин, а остальное представляет сложную смесь органических веществ, включая белки, полипептиды, низкомолекулярные азотистые соединения, углеводы, различные органические кислоты и, в зависимости от штамма продуцента, то или иное количество пигмента. Для выделения пенициллина из этой сложной смеси можно пользоваться методами, основанными на адсорбции, экстракции или осаждении.
В промышленности извлечение активного вещества из нативного раствора основано на экстракции не смешивающимся с водой растворителем при подавленной диссоциации карбоксильной группы пенициллина. В растворитель, кроме пенициллина, переходит большая часть органических кислот. Минеральные загрязнения, большая часть азотистых соединений и других органических веществ остаются в водной фазе, так что в результате экстракции чистота продукта увеличивается в 4-6 раз.
К растворителям, применяемым для экстракции пенициллина, предъявляются следующие основные требования:
1) малая растворимость в воде;
2) отсутствие взаимодействия с пенициллином;
3) низкая упругость пара при температуре 5—30°С;
4) возможность регенерации при температуре не выше 120 — 140°;
5) низкая стоимость.
С учетом этих и ряда других показателей основными растворителями-экстрагентами были приняты бутилацетат и амилацетат.
При кислых значениях рН пенициллин нестабилен, поэтому при экстракции пенициллина в органический растворитель необходимо строго контролировать рН, поддерживая его в пределах 1,9-2,0, проводить экстракцию в возможно короткое время, охлаждать жидкости.
При экстракции пенициллина из нативного раствора образуются весьма стойкие, трудноразделяемые эмульсин, что обусловлено наличием в нативном растворе поверхностно-активных веществ. Это требует применения специальных дезэмульгаторов. Обычно для этой цели применяют анионные детергенты, например сульфированные жирные или нафтеновые кислоты. Обычно выбор детергента определяется его доступностью и экономическими соображениями. Для разделения эмульсии в экстракторах-сепараторах, как правило, достаточно добавлять к нативному раствору 0,05—0,1% детергента.
На стадии экстракции пенициллина из нативного раствора используются либо многоступенчатые экстракторы-сепараторы типа «Лувеста» и «Россия», либо двухступенчатая схема экстрагирования (контактирование подкисленного нативного раствора с бутилацетатом в специальных смесителях и разделение эмульсии на центробежных сепараторах типа САЖ-3).
Применение эффективных центробежных экстракторов-сепараторов (с производительностью 4000—5000 л/час), обеспечивающих по крайней мере две ступени экстракции в одной машине и хорошее разделение фаз, сводит до минимума время пребывания пенициллина в кислой водной среде и, следовательно, повышает выход антибиотика. Применение двухступенчатой схемы при экстракции пенициллина из нативного раствора, безусловно, нежелательно не только вследствие более длительного времени пребывания пенициллина в неблагоприятных условиях в этом случае, но и вследствие того, что применение сепараторов САЖ-3 (производительность которых колеблется в пределах 800— 1000 л/час) не всегда обеспечивает достаточно полное разделение фаз. Это влечет за собой ухудшение качества бутилацетатного экстракта (загрязнение нативным раствором) и увеличение потерь бутилацетата с отработанным нативным раствором. Соотношение фаз при проведении бутилацетатной экстракции пенициллина из нативного раствора составляет 1,0:0,3—0,45, температура 4—3°С.
После проведения бутилацетатной экстракции пенициллина из нативного раствора производят извлечение пенициллина из бутилацетатного экстракта водным раствором бикарбоната натрия или буферным раствором при рН 6,6—7,2. На этой стадии также применяют многоступенчатые экстракционные машины или используют двухступенчатую противоточную экстракцию с разделением эмульсии на сепараторах с отношением растворительно-водная фаза 1.0:0,35. Выход по бутилацетатной и буферной экстракциям составляет около 90-92%.
Для дальнейшей очистки пенициллин повторно извлекают из буферного экстракта органическим растворителем (чаще всего бутилацетатом или хлороформом) при рН 2,0. Процесс ведется аналогично бутилацетатной экстракции из нативного раствора. Эта стадия технологически оформляется также с применением многоступенчатых экстракционных машин или осуществляется в виде двухступенчатой противоточной экстракции с разделением фаз на сепараторах. Выход составляет около 86% от количества пенициллина, содержащегося в нативном растворе.
Весь экстракционный процесс извлечения и химической очистки пенициллина проводится по непрерывной схеме.
3.2.5 Выделение кристаллических солей пенициллина
Наиболее надежным методом, обеспечивающим получение кристаллического пенициллина хорошего качества, является выделение бензилпенициллина из бутилацетатного экстракта в виде концентрированного водного раствора калиевой соли с последующим упариванием воды с бутанолом под вакуумом, что приводит к кристаллизации калиевой соли из бутилового спирта.
Этот процесс имеет следующую технологическую последовательность:
1. Обезвоживание бутилацетатного экстракта путем охлаждения до —16-18°С с последующей фильтрацией от льда. Удаление пигментных загрязнений обработкой активированным углем и фильтрацией на охлажденном друк-фильтре.
2. Получение концентрата калиевой соли бензилпенициллина экстракцией 0,56—0,6 н раствором едкого кали.
3. Стерилизующая фильтрация концентрата калиевой соли и упаривание под вакуумом с бутиловым спиртом (2,5 объема) при температуре 16—26° и остаточном давлении 5—10 мм рт. ст. Объем кубового остатка должен составлять не более 60—80% объема загруженного концентрата. Добавление бутанола к концентрату при упаривании под вакуумом связано с тем, что бутанол с водой образует смесь, кипящую при более низкой температуре по сравнению с температурой кипения воды. Отгонка воды проводится сравнительно в мягких условиях, вследствие чего возможность инактивации пенициллина уменьшается. После удаления воды и большей части бутилового спирта калиевая соль бензилпенициллина кристаллизуется,
4. Фильтрация осадка калиевой соли бензилпенициллина на фильтрующей центрифуге и промывка осадка безводным бутиловым спиртом.
5. Гранулирование полученной пасты и сушка калиевой соли в вакуум-сушильных шкафах при температуре 75—80° и остаточном давлении 10—20 мм рт. ст. При этом получается калиевая соль бензилпенициллина в виде белого мелкокристаллического порошка с активностью содержанием бензилпенициллина порядка 95% и выходом 70% от количества антибиотика в нативном растворе.
Важнейшим требованием, предъявляемым к получаемому сухому порошку пенициллина, является его полная стерильность. Термическая обработка препарата недостаточна. Стерильность может быть обеспечена лишь при проведении заключительных стадий процесса в строго асептических условиях, исключающих возможность заражения продукта микроорганизмами и их спорами. Поэтому, начиная со стерилизующей фильтрации концентрата и бутанола, все операции проводятся в изолированных стерильных помещениях и в стерильной аппаратуре. Для обеспечения условий асептики осуществляется весь комплекс необходимых санитарных и технологических мероприятий.
Перед регенерацией бутилацетат и бутанол, применяемые в процессе выделения и химической очистке пенициллина, промывают раствором щелочей для удаления примесей кислот (продуктов инактивации пенициллина, фенилуксусной кислоты).
3.3 Отходы производства
Основные отходы, образующиеся в результате выделения и химической очистки антибиотиков, следующие: отработанные нативные растворы, водные маточные и промывные растворы, водные растворы кислот и щелочей после регенерации ионообменных смол, отработанный активированный уголь, кубовые остатки после регенерации растворителей. В этих отходах вредную долю составляют антибиотики и продукты их деструкции, а также органические растворители.
Принципиальные задачи совершенствования технологии получения антибиотиков из нативных растворов с точки зрения сокращения отходов производства заключаются в повышении выхода целевых продуктов и тем самым снижении потерь антибиотика, снижении расходов сырья на стадиях и повышении эффективности регенерации органических растворителей.
Существенное снижение потерь антибиотиков в процессе их выделения может быть достигнуто путем решения комплекса задач: усовершенствование процесса ферментации с целью повышения качества культуральных жидкостей; проведение эффективной очистки нативных растворов от примесей, затрудняющих процессы выделения антибиотиков; сокращение числа технологических стадий; уменьшение длительности процессов; использование эффективного высокопроизводительного оборудования.
Так, применение эффективной очистки и подготовки нативных растворов пенициллина позволяет повысить концентрацию перерабатываемых нативных растворов на 30-40% и открывает возможность применить сокращенную схему экстракционной очистки антибиотика, что снижает примерно вдвое расход бутилацетата при экстракции и активированного угля на очистку экстракта. При этом достигается уменьшение потерь антибиотика на 15-30%, что соответственно снижает количество поступающих в отходы антибиотика и продуктов деструкции.
Одной из важнейших проблем производства антибиотиков является утилизация и обезвреживание мицелиальных отходов. Мицелиальные отходы образуются в результате отделения жидкой фазы культуральной жидкости.
Часть образующихся мицелиальных отходов утилизируется в сельском хозяйстве. Это мицелиальные массы продуцентов пенициллина, тетрациклина и хлортетрациклина. Применение мицелиальных отходов для кормления крупного рогатого скота увеличивает среднесуточные привесы на 16-58%. Расход кормов при этом снижается на 10-30%.
Однако более двух третей образующегося мицелия утилизируется в отвалы, систему сточных вод или сжигается, что нельзя назвать приемлемым как с позиции загрязнения почв и загрузки очистных сооружений, так и с точки зрения нерационального к этому типу отходов, содержащих достаточное количество ценных веществ.
3.4 Охрана окружающей среды
Основные газовые выбросы в атмосферу предприятий по производству антибиотиков, содержащие вредные вещества, включают, кроме воздушных выбросов общеобменной и местной вентиляции, технологические воздушные выбросы при биосинтезе антибиотиков, выбросы котельных и некоторых других вспомогательных производств. Различными способами очистки обеспечивается улавливание около 60% вредных веществ, отходящих от всех источников загрязнения.
Газообразные вредные вещества состоят в основном из окиси углерода (77,4%), сернистого газа (15,2%) и окислов азота (7,4%).
К специфическим для производства антибиотиков жидким и газообразным продуктам относятся пары органических растворителей, составляющие 24,3% от общей суммы выбрасываемых веществ (табл. 3).
Таблица 3 – Качественный и количественный состав органических растворителей в воздушных выбросах производства антибиотиков
| Наименование классов и веществ | Содержание растворителя в выбросе в % от общей суммы выбрасываемых растворителей |
| 1. Спирты | 55,27 |
| Этиловый спирт | 26,26 |
| Бутиловый спирт | 16,69 |
| Метиловый спирт | 8,20 |
| Изопропиловый спирт | 4,00 |
| Пропиловый спирт | 0,07 |
| Изооктиловый спирт | 0,05 |
| 2. Сложные эфиры | 32,22 |
| Бутилацетат | 30,66 |
| Этилацетат | 1,56 |
| 3. Ацетон | 9,26 |
| 4. Хлорпроизводные углеводородов | 2,88 |
| Хлористый метилен | 2,37 |
| Четыреххлористый углерод | 0,39 |
| Трихлорэтилен | 0,09 |
| Хлороформ | 0,03 |
| 5. Углеводороды | 0,32 |
| Бензин | 0,27 |
| Бензол | 0,05 |
| 6. Простые эфиры | 0,05 |
| Диэтиловый эфир | 0,04 |
| Диметиловый эфри | 0,01 |
Кроме того, в воздушных выбросах присутствует целый ряд примесей паров различных веществ, составляющих 0,4% от общей суммы выбрасываемых в атмосферу жидких и газообразных продуктов. Среди них преобладает хлористый водород, пары соляной кислоты, формальдегид и трикрезол.
Неспецифические для производства антибиотиков твердые вещества в выбросах улавливаются газопылеочистными установками на 90%, газообразные выбросы котельных рассеиваются с помощью высоких труб. Специфические для производства антибиотиков твердые веществ из воздушных выбросов на 92,5%, органические растворители – на 10%, обезвреживается 5,4% от объема воздушных выбросов при биосинтезе антибиотиков.
